Sommaire
- Biofilms : Les bactéries résistent !
- Identification individuelle par séquençage d’une bactérie et d’une moisissure présentes en mélange
- Lyophilisation : comment utiliser la mesure manométrique de la température (MTM) pour comprendre l’influence de la température de nucléation sur la résistance au transfert de matière d’un produit
- L’activité des désinfectants sur les champignons communs de salles propres
- Cahier Pratique : Mise en place d’un système de biodécontamination sur une unité de biotechnologie
- Interview d’Alexandre Guerry, Project Manager R&D Cytosial Biomedic
- De nouveaux chemins dans la mesure Carbone Organique Total (COT ou TOC)
- Cytotoxic Chemical contamination risks and protective measures at hospital pharmacies
- Management – Rien n’est permanent sauf le changement, Partage d’expérience et de petits trucs…
Aujourd’hui, dans les salles propres dotées d’équipement pharmaceutique, de matériel de biotechnologie et d’instruments médicaux, on observe une prévalence croissante des moisissures qui peut donner lieu à des campagnes de surveillance environnementale ou à des arrêts des opérations. Bien que la fermeture du site constitue le pire des cas, l’isolement fréquent des champignons au sein d’une salle propre peut présager d’un réservoir potentiel de contamination qui peut générer des problèmes sur le long terme.
De nombreuses sociétés pharmaceutiques et de biotechnologie font face à certains défis quand il s’agit de définir les limites acceptables des moisissures dans le cadre de leurs opérations en salle propre. Bien qu’un seuil de zéro ne soit pas réaliste, il existe une propension à définir des niveaux très faibles de moisissures dans la plupart des opérations afin de minimiser les problèmes à venir. Afin de maintenir les chiffres de moisissures sous ces niveaux cibles, il est essentiel de choisir des désinfectants qui démontrent une activité satisfaisante sur les champignons communs de salles propres. Les spores fongiques, comme les spores bactériennes peuvent constituer des challenges de taille pour de nombreux désinfectants couramment utilisés. Cet article donne un aperçu d’exemples de contrôles de contamination standard et propose une étude de l’activité de plusieurs désinfectants et sporicides vis-à-vis des champignons communs que l’on trouve lors d’opérations en salle propre sur du matériel pharmaceutique, des équipements de biotechnologie ou des instruments médicaux.
Études de cas
Au fil des années, des problèmes de moisissures dans les salles propres, les chambres froides, les zones contrôlées, les espaces interstitiels et les nouvelles salles propres ont été signalés (1). Des moisissures comme l’Aspergillus proviennent de diverses sources au sein de la salle propre, comme les plaques de bas de porte, les sacs, les incubateurs, les boîtes, les marqueurs, l’équipement d’intervention, les roues de chariot, les carreaux du plafond, le sol qui se dégrade et, dans certains cas, des dispositifs à jet haute pression pour l’application de germicides (1). Les vibrations de la construction, des systèmes de gicleurs et des fixations de luminaires mal conçus ont également été l’origine d’invasions de moisissures dans les salles propres. Récemment, plusieurs sociétés pharmaceutiques et fabricants de vaccins en Europe ont connu une augmentation de la présence de moisissures due à une augmentation des températures ambiantes et à des problèmes liés à des objets amenés dans ces salles. Comme les sources de contamination fongique sont extrêmement variées, il est impératif de prendre en considération tous les facteurs potentiels qui peuvent contribuer aux problèmes de moisissures, y compris la conception et la maintenance de l’installation, les objets amenés dans les salles blanches, les pratiques du personnel et l’adéquation des produits utilisés pour le nettoyage et la désinfection.
Ces derniers temps, l’Aspergillus, le Penicillium, le Trychophyton, le Stachybotrys ainsi que d’autres moisissures ont généré des problèmes d’invasion microbienne significative qui ont eu des impacts négatifs sur la production. Par exemple, l’Aspergillus niger a récemment engendré 35 millions de dollars de frais de rénovation chez un gros fabricant de médicaments génériques par voie parentérale sur la Côte Ouest des Etats Unis. Ce fabricant a dû rénover ses panneaux en acier inoxydable et remplacer les sols pour solutionner les problèmes liés à des foyers de moisissures endémiques. Autre exemple récent, l’arrêt pendant plusieurs jours de la production dans une salle propre à cause d’une infestation importante de Trychophyton attribuée à un opérateur qui souffrait du pied d’athlète. Le Penicillium constitue une autre espèce de moisissure fréquemment isolée sur la base des données de surveillance environnementale au cours des opérations en salle propre. Il y a quelques années, un site avait recensé un certain nombre d’isolat de l’espèce Penicillium générant des infestations au cours de ses opérations, ce qui a mené à une recherche longue et très coûteuse. Le Stachybotrys a également posé problème dans certains établissements. Un site ayant recours à un dispositif de vaporisation par jet haute pression dans ses salles propres pour l’application de désinfectants a finalement fait des trous dans les cloisons et parois murales, ce qui a généré des infestations endémiques de Stachybotrys et d’Aspergillus.
Du matériel de colmatage a été placé sur les murs pour résoudre les problèmes, mais le nombre de trous et de colmatages sur le site était si important que le problème n’a jamais pu être résolu.
Ces exemples illustrent l’étendue des problèmes de moisissures et montrent pourquoi il est important d’utiliser les produits chimiques adéquats contre les moisissures afin garder ces infestations sous contrôle et de minimiser les frais des mesures correctrices ainsi que les pertes de productivité. À cette fin, une étude a été mise sur pied afin de fournir des données à propos des produits chimiques adéquats pour éliminer les champignons spécifiques aux salles propres. Cette étude a comparé l’activité de six désinfectants différents contre cinq espèces de moisissures très répandues.
Matériel et méthodes
Culture et préparation de micro-organismes Des cultures d’Aspergillus niger ATCC 16404, d’Aspergillus fumigatus ATCC 96918, de Penicillium notatum ATCC 10108, de Trichophyton mentagrophytes ATCC 9533, et de Stachybotrys chartarum ATCC 16275 ont été réalisées sur de la gélose de Sabouraud Dextrose (SDA) pendant une période de 7 à 10 jours à 24 °C. Le jour du test, 10 millilitres de tampon stérile de Butterfield ont été ajoutés à chaque tube de culture et on a délicatement frotté les particules de mycélium de la surface de la gélose à l’aide d’une oese stérile dans la suspension. Ces suspensions furent ensuite pipetées dans des dispositifs stériles pour broyage de tissus et furent macérées jusqu’à ce qu’à obtenir une certaine consistance. L’inoculum microbien de travail variait d’un organisme à l’autre selon une plage d’environ 5 x 104 – 3 x 106 CFU/ml.
Une mesure du temps pour l’élimination a été réalisée pour évaluer l’activité de divers désinfectants sur chaque organisme fongique. Dans le cadre de cette méthode, cent microlitres d’inoculum préparé est pipeté dans dix millilitres de désinfectant pour produire un ratio de 1:100. Pour le contrôle de l’inoculum, chaque organisme est également complété de dix millilitres de tampon. Cent millilitres de suspensions sont retirés et neutralisés dans 9,9 millilitres de milieu approprié à chacun des trois points suivants: 30 secondes, 60 secondes et 120 secondes.
Les valeurs log10 des données CFU/ml ont été calculées pour les contrôles de base et les articles de test. Les valeurs de réduction log10 représentent la différence entre le contrôle de base moyen log10 et le log10 des valeurs des articles en test.
Résultats
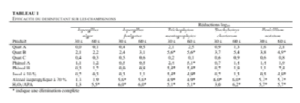
L’étude initiale a évalué l’activité de 8 produits disponibles sur le marché dans une étude de mesure de la durée d’élimination dans une suspension sur un large spectre de champignons, avec des temps de contact de 30 et 60 secondes.
Les résultats ont indiqué une plage d’activité qui n’avait pas directement été corrélée à un type d’ingrédient actif spécifique, mais qui dépendait fortement de la formule. 5 produits sur 8 ont été relativement inefficaces comparés aux autres. Ces 5 produits moins efficaces étaient le Phénol A (phénol à pH élevé), le Phénol B (phénol à pH faible), le Quat A (produit ammonium quaternaire avec 21 % d’alcool isopropylique), le Quat C (composés d’ammonium quaternaire/Biguanide), et de la Javel à 10 %. Cependant, deux d’entre eux ont pu éliminer complètement un champignon spécifique, le Trichophyton mentagrophytes.
En ce qui concerne le large spectre de produits, le Trichophyton mentagrophytes a généralement été le plus facile à tuer, alors que l’Aspergillus niger a été le plus difficile à éliminer. La Javel a été moins efficace que ce que l’on attendait. Initialement, nous pensions que de la Javel à 10 % pourrait être un des produits les plus performants, bien que nous sachions que l’hypochlorite de sodium présentait des problèmes de stabilité, de sélectivité et de compatibilité avec certains matériaux.
Cependant, la plus faible activité de la Javel, tout particulièrement à des temps de contact plus courts, peut être le résultat de la présence d’éléments fongiques ou d’autres matières organiques dans la suspension de test (2).
Les trois produits démontrant la meilleure activité à large spectre, par ordre d’activité croissante, étaient :
1. Quat B (ammonium quaternaire concentré)
2. Alcool isopropylique à 70 %
3. Peroxyde d’hydrogène/acide peracétique (H2O2/APA)
La performance du Quat B semble directement liée à sa formule unique, comparée à d’autres solutions d’ammonium quaternaire utilisées lors de notre test. Ceci indique que la formule de produits quaternaires spécifiques peut avoir une grande influence sur leur efficacité sur certains champignons cibles.
De plus, d’autres résultats de test suggèrent qu’une rotation dans l’utilisation de ces trois produits pourrait garantir à l’utilisateur une couverture antimicrobienne plus complète contre les multiples espèces de moisissures.
Tests supplémentaires
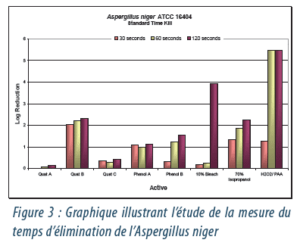
Les résultats de l’étude initiale de la mesure du temps d’élimination dans la suspension ont montré que l’Aspergillus niger représentait l’organisme/le champignon le plus résistant pour les produits à large spectre utilisés dans leur ensemble. Pour dessiner davantage le profil de résistance de l’Aspergillus niger face à ces nombreux produits, une série d’expériences en suspensions supplémentaires ont été menées avec un temps de contact rallongé à 120 secondes.
La figure 3 montre les résultats de ces études et nous procure des informations très précieuses. La performance de nombreux produits (Alcool isopropylique à 70 %, Phénol A, Quat A et Quat C) semblait baisser considérablement ou rester au même niveau par rapport à ce que nous avions observé lors des 30 premières secondes d’activité. Cette observation pourrait être due à la variation naturelle au sein d’une population fongique. La Javel à 10 % présentait un retard initial très long et était incapable d’arriver à une élimination complète avant un temps de contact de deux minutes. Cependant, l’activité de l’H2O2/APA a tué rapidement la population entière d’Aspergillus niger en 60 secondes. Cette étude a confirmé qu’une rotation avec l’utilisation de l’alcool isopropylique à 70 %, du Quat B et de l’H2O2/ APA pouvait couvrir les exigences d’activité pour tuer efficacement un large spectre d’organismes fongiques. Les formules phénoliques testées ici ont démontré une activité contre l’Aspergerillus niger supérieure à deux des produits d’ammonium quaternaire mais inférieure au Quat B ou à l’H2O2/APA. Néanmoins, l’on sait que les composés phénoliques ont démontré une excellente activité bactéricide et virucide, et sont utilisés de manière routinière lors des opérations en salle propre. De par son activité plus élevée et sa meilleure compatibilité avec les matériaux, la formule d’H2O2/APA est généralement préférée à la Javel à 10 %.
Conclusion
Cette étude a révélé que différents agents antimicrobiens et formules antimicrobiennes démontrent une activité variable contre les moisissures. Il semble donc prudent de choisir un produit chimique antimicrobien adapté à des isolats de moisissures spécifiques des problématiques liées aux opérations dans nos salles propres. Les produits H2O2/APA sont largement utilisés dans l’industrie aujourd’hui pour éliminer à la fois les moisissures et les spores bactériennes dans les salles propres. Dans cette étude, les mélanges H2O2/APA ont démontré une excellente activité globale sur les espèces de moisissures testées. Les données indiquent également que d’autres formules démontrent une activité fongique, bien que cette activité ne soit pas directement mise en relation avec le type d’actif.
Un programme abouti de nettoyage et de désinfection contrôle les populations de moisissures et évite les infestations qui peuvent avoir un impact sérieux sur les opérations et la productivité. La pratique approuvée dans les salles propres aujourd’hui consiste à utiliser un ou plusieurs désinfectants sur les murs, les sols, les plafonds et l’équipement, et d’appliquer un sporicide pour éliminer les spores fongiques et bactériennes (3). Il faut noter que l’industriel doit avoir conscience que les rotations proposées ci-dessus permettent un maintien de la salle propre et de son contenu sous contrôle en continu. Toutes démarches palliatives préventives en cas de suspicion d’excursion à l’aide d’autres technologies d’apport ponctuel de sporicide en phase gazeuse ou nébulisée doivent être considérées comme un constat d’échec et un surcoût d’exploitation que ne manqueront pas de relever respectivement les auditeurs internationaux et les directions de site.
En plus de la prise en considération de facteurs comme la conception et la maintenance de l’installation, les pratiques du personnel, la formation et les objets amenés dans les salles propres, il est essentiel d’investir dans la recherche des produits antimicrobiens efficaces contre des isolats spécifiques de moisissures. Ces activités contribueront à limiter la croissance fongique et ses conséquences nuisibles.

Jim POLARINE – STERIS CORPORATION
jm_polarine@steris.com

Frédéric BAR – STERIS CORPORATION
frederic_bar@steris.com
Partager l’article
Références
1. Bartnett, C., Polarine J., and Lopolito P. (2007) Control Strategies for Fungal Contamination in Cleanrooms Controlled Environments September 2007
2. Klein, D.A. et al. (May 2006) Disinfectant Testing Against Aspergillus niger. Poster presented at: Annual Meeting of the American Society of Microbiologists. Poster Q-407.
3. USP 37 <1072> Disinfectants and Antiseptics bactériennes dans les salles propres. Dans cette étude, les mélanges H2O2/APA ont démontré une excellente activité globale sur les espèces de moisissures testées. Les données indiquent également que d’autres formules démontrent une activité fongique, bien que cette activité ne soit pas directement mise en relation avec le type d’actif.