Juin 2013
La Vague n°38
Particulièrement PARTICULES
Sommaire
- Risques particules et verre dans les produits injectables.
- De la prévention à la détection des particules visibles.
- La maitrise de la contamination particulaire dans la production de bouchons en élastomère.
- Confluences particulaires, de la visibilité partagée.
- L’analyse de risque partagée entre fournisseurs et utilisateurs : une garantie de sécurité pour les patients.
- Revue des Pratiques d’Inspection Visuelle.
Revue des Pratiques d’Inspection Visuelle
Dans l’industrie pharmaceutique des injectables et des solutions ophtalmiques, les pratiques d’inspection visuelle revêtent de multiples facettes en fonction de facteurs tels que la diversité des présentations (solutions, suspensions, émulsions, lyophilisats) des articles de conditionnement (seringues, ampoules, flacons, cartouches), des volumes et de la valeur des produits. Pourtant, un dénominateur commun reste : il s’agit d’un sujet « chaud » tant pour des aspects régulatoires que business. D’après les différentes monographies, 100% des unités produites doivent être inspectées. Dans ce contexte, l’inspection répond à des normes, et certaines pratiques communes peuvent être identifiées. Dans ce contexte, un groupe de travail A3P s’est constitué pour analyser et dégager des dénominateurs communs.
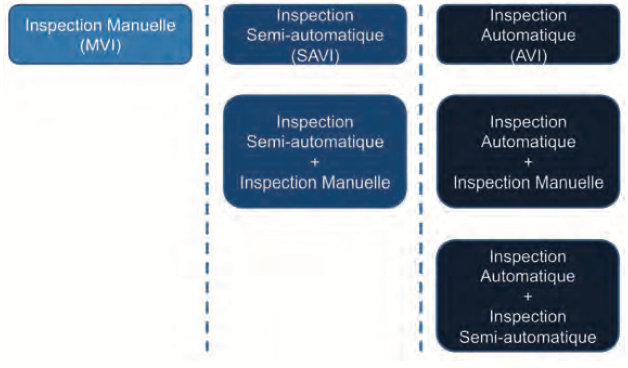
1. On distingue 3 approches principales :
L’inspection manuelle (MVI) – L’inspection Semi-automatique (SAVI) – L’inspection automatique (AVI). Ces 3 approches sont parfois dupliquées et/ou combinées (par exemple plusieurs inspections automatiques avec une inspection manuelle) (voir schéma ci-dessous) :
Une tendance récente est d’associer d’autres tests complémentaires à l’IV tels que les tests de fêlures traversantes par analyse spectrale, arc électriques ou pression différentielle. Les défauts à détecter sont dans le domaine du visible pour l’œil humain, le visible ne se réduit pas qu’a une notion de taille de l’objet supérieur à 50 μm. En effet, un défaut visible désigne un défaut inspecté de façon probabilistique par un opérateur qualifié puis certifié dans des conditions de travail standard sur un poste dédié. Ce peut être par exemple une particule, une fêlure, un défaut sertissage non détecté à 100% par l’homme. Cela induit que pour tout défaut visible un taux de détection probabilistique peut lui être associé (QF). (Ref. n°1)
2. Quels sont les objectifs de l’IV ?
- C’est avant tout une attente réglementaire pour tout produit injectable permettant de garantir la qualité d’un produit destiné à être injecté (innocuité pour le patient, stabilité dans le temps).
- Détecter et éliminer de façon probabilistique des défauts visibles.
- Mesurer les occurrences de défauts.
- Mettre en place une amélioration continue sur la base de détermination des causes de défaut identifiés comme étant intrinsèques ou extrinsèques au procédé de fabrication du produit (évaluation qualitative).
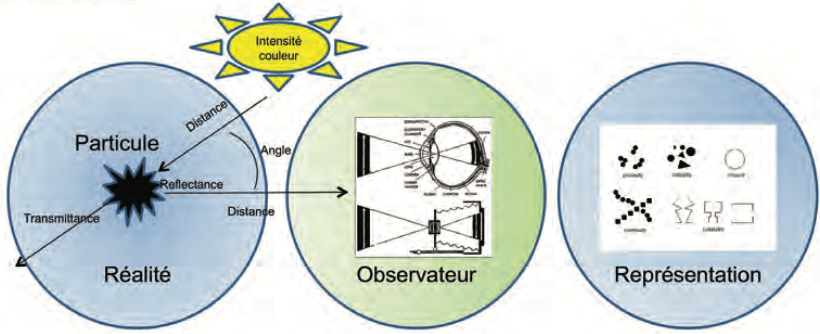
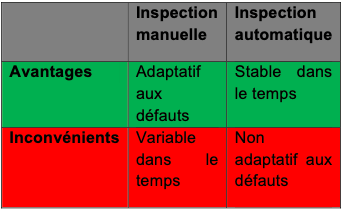
Un des paradigmes de l’inspection visuelle est que l’on prend une décision non à partir de la réalité elle-même mais plutôt à partir d’une représentation d’une projection optique de la réalité. La capacité d’interprétation des opérateurs peut être soit un avantage mais cela présente aussi des inconvénients :
Ainsi, beaucoup de paramètres se révèlent comme critiques pour l’inspection visuelle:
- Acuité visuelle des opérateurs / résolution caméra et optiques,
- Éclairages et angles de projection,
- Distance d’inspection,
- Qualité et stabilité des éclairages,
- Mouvement des unités,
- Standardisation de l’inspection
- La taille des défauts, en particulier celle des particules,
- Le volume à inspecter,
- La certification et l’expérience des opérateurs / qualification des machines,
- Concentration et fatigue des opérateurs,
- Cadences à respecter, en lien avec le processus de qualification des opérateurs et les attentes pharmacopées (4-5 s par fond),
- Nombre de défauts à inspecter,
- Articles de Conditionnement Primaires dont la nature et la forme du contenu,
- Occurrence de défauts connus ou non connus des opérateurs (cas d’apparition de nouveaux défauts).
3. Les 3 catégories d’inspection
- Inspection manuelle : elle reste la ligne de référence pour les autres pratiques d’inspection, elle se doit donc d’être bien maitrisée avant de choisir une technique alternative. Une guidance OMS (Ref. n°2) ainsi que les monographies US, Eur. Japan décrivent des conditions opératoires très proches ; on retient souvent 10 secondes d’inspection sur fond noir et sur fond blanc avec un éclairage entre 2000 et 3750 Lux, mais des rationnels spécifiques peuvent justifier toute autre approche. Une procédure reprend en général la description précise de la gestuelle pour la présentation des défauts, la description du flux d’inspection et de contrôle des cadences. La revérification des défauts est effectuée soit in situ en production soit à postériori par une équipe dédiée. 2 types de contrôles sont généralement appliqués ; les échantillonnages AQL et les cartes de contrôle. Enfin, tout ce processus doit alimenter une boucle d’amélioration continue qui est bien repris dans la monographie USP <790> (Ref. n°1).
- L’inspection semi-automatique ne diffère pas fondamentalement de l’IV manuelle, si ce n’est que les opérations suivantes sont automatisées : présentation de l’Objet (rotation), éclairage, convoyage, magnification optionnelle. Typiquement les cadences peuvent être améliorées mais cela nécessite une certaine stabilité et maturité dans les processus d’inspection. Ce type de mirage est plutôt indiqué soit pour des produits dont le procédé de remplissage est stabilisé (historique) et a permis de déterminer les défauts les plus courants (constitution des défauthéques), soit il est indiqué dans le cadre d’une inspection secondaire des unités éjectées après inspection automatique
- L’AVI se distingue quant à elle par une grand diversité de parc machine qui tient à l’évolution constante des technologies. Cependant, les séquences suivantes restent les mêmes : présentation de l’Objet / Eclairage / Acquisition de l’image / prétraitement pour réduire l’information / Traitement d’image / Post traitement pour aider la décision / Décision / comptage et archivage des résultats. Cette séquence peut se faire à haute cadence jusque vers 36 000 unités par heure, dans ce contexte la complexité des machines requièrent des compétences en mécanique, automation et vision tant chez le fournisseur que chez l’utilisateur final.
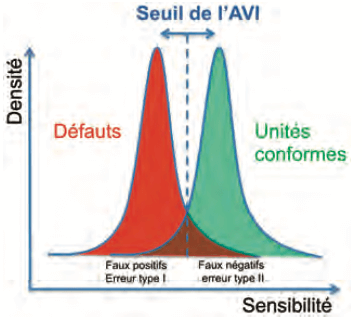
La mise au point de l’inspection automatique repose sur le schéma suivant :
Si une population de défauts est considérée, elle ne représente que quelques ppm, elle peut se représenter par la courbe de gauss en rouge. Le principe de l’inspection sera d’éliminer un maximum de défauts de façon à être au moins équivalente à l’inspection manuelle, considérée en principe comme méthode de référence. En général, la littérature Knapp & Kushner (Ref. n°3) donne un taux de détection d’environ 70% pour des particules en inspection manuelle, des études récentes valident bien ce seuil pour des défauts probabilistiques avec des flacons et des seringues (Ref. n°4). Cependant, lorsque des défauts sont éjectés, des bonnes unités sont aussi éjectées de façon inhérentes (courbe de gauss en vert), ce sont les éjections ou « faux rejets » qui correspondent une erreur de type I (risque fournisseur). Les facteurs pouvant affecter les éjections sont par exemple la qualité de surface du verre, la densité optique des suspensions, les bulles d’air générées par les conditions opératoires (convoyage des unités, température des solutions favorisant leur dégazage lors de l’inspection), la poudre lyophilisée dans ce contexte les 2 courbes de gauss se chevauchent davantage et les faux rejets augmentent. Pour les produits lyophilisés ou les suspensions très denses, il conviendra de re-évaluer les performances de l’inspection manuelle. Alors rentrent en jeux des outils de vision très spécifiques pour séparer au mieux ces 2 populations.
- Afin de contrôler le processus d’inspection à postériori, quel que soit le procédé appliqué, 2 outils sont utilisés :
Les échantillonnages statistiques ou
« AQL », pour contrôler la qualité de l’inspection, par exemple sur une base ISO 2859-1. Le contrôle AQL reste d’un point de vue réglementaire, libératoire pour le produit car il indique la quantité d’unités défectueuses dans la totalité des unités acceptées du lot qui a été miré. - Les cartes de contrôle, pour monitorer la qualité du lot inspecté. Les résultats des cartes de contrôles permettent d’évaluer la relation qualité du lot après remplissage vis-à-vis de la capacité filtrante du système de vision en définissant des limites d’investigation basées sur l‘historique d’occurrence des défauts. L’analyse fine des tendances permet de bien connaitre son procédé d’inspection et d’adapter la stratégie de mirage pour des lots de produits ayant des profils de résultats atypiques.
La validation peut être suivie d’un accompagnement de ces contrôles sur les premiers lots.
Un principe de validation est basé sur la méthode Knapp et Kushner (Ref. n°3) qui considère une méthode de référence (l’inspection manuelle) et une méthode secondaire (l’inspection automatique), le critère de validation est en général d’avoir une performance moyenne d’inspection automatique au moins supérieure ou équivalente à la performance moyenne de l’inspection manuelle (schéma ci-dessous) :
Afin de contrôler le processus d’inspection à postériori, quel que soit le procédé appliqué, 2 outils sont utilisés :
- Les échantillonnages statistiques ou « AQL », pour contrôler la qualité de l’inspection, par exemple sur une base ISO 2859-1. Le contrôle AQL reste d’un point de vue réglementaire, libératoire pour le produit car il indique la quantité d’unités défectueuses dans la totalité des unités acceptées du lot qui a été miré.
- Les cartes de contrôle, pour monitorer la qualité du lot inspecté. Les résultats des cartes de contrôles permettent d’évaluer la relation qualité du lot après remplissage vis-à-vis de la capacité filtrante du système de vision en définissant des limites d’investigation basées sur l‘historique d’occurrence des défauts. L’analyse fine des tendances permet de bien connaitre son procédé d’inspection et d’adapter la stratégie de mirage pour des lots de produits ayant des profils de résultats atypiques.
La validation peut être suivie d’un accompagnement de ces contrôles sur les premiers lots.
Un principe de validation est basé sur la méthode Knapp et Kushner (Ref. n°3) qui considère une méthode de référence (l’inspection manuelle) et une méthode secondaire (l’inspection automatique), le critère de validation est en général d’avoir une performance moyenne d’inspection automatique au moins supérieure ou équivalente à la performance moyenne de l’inspection manuelle (schéma ci-dessous) :
Ainsi, La méthode de validation K&K est basée sur la comparaison des performances moyennes des 2 méthodes d’inspection. L’objectif de la validation n’est pas de déterminer une corrélation pour chaque défaut entre l’inspection manuelle et automatique (Ref. n°3). En effet, lorsque l’on considère les 10 opérateurs qui réalisent l’inspection manuelle il n’y a pas de contingence significative (Ref. n°4). Cependant, l’étude et la documentation des taux de détection pour chaque défaut peuvent aider à la compréhension de l’inspection automatique.
A l’origine cette méthode K&K a été développée pour les particules, mais elle est parfois utilisée pour d’autres défauts probabilistiques.
D’autres approches de validation sont basées sur l’analyse des occurrences qui permet de passer des contrôles AQL, cette approche demande un procédé historique plus stable.
Dans la maitrise du processus d’inspection automatique, la maintenance des systèmes vision doit permettre de prouver que l’on reste toujours dans un état machine validé. Une attention particulière est apportée au contrôle des alignements, des focus et des intensités lumineuses. Le développement d’une stratégie de contrôle vision doit permettre de documenter que l’on retourne dans un état validé.
Le kit journalier est une pratique utile lorsque la machine requiert des réglages quotidiens qui nécessitent de démontrer que l’on reste dans un état validé. En revanche, sur des systèmes plus modernes ou aucun paramètre n’est changé au quotidien et pour lesquels tous les paramètres critiques sont contrôlés en permanence par alarme, la fonctionnalité de ce test journalier peut être revue.
Une des clefs reste la gestion de la bibliothèque de défaut (Ref. n°5) ainsi que la formation qualification des opérateurs de mirage à la détection des défauts. Une boucle d’amélioration continue doit l’alimenter tant sur les occurrences que sur les caractérisations. Ceci est bien repris dans le draft USP <1790>. Cette gestion permet d’avoir un processus de création et de gestion des kits de défauts très robuste qui va soutenir toutes les validations. La création des kits peut être centralisée dans un groupe spécifique.
Dans le cadre de l’A3P, un groupe de travail constitué de représentants de l’industrie s’est créé : l’objectif est de discuter et partager nos pratiques d’inspection visuelle afin de trouver des dénominateurs communs et des bonnes pratiques. Un questionnaire balayant toutes les pratiques d’inspection a été élaboré, il est téléchargeable sur le site www.a3p.org dans l’espace Evénement / Particules Visibles Vaudreuil 4 juillet 2013.
Nous vous invitons à le compléter et le partager, 15 sites ayant déjà participé, nous communiquerons les résultats le 4 juillet 2013 lors de notre journée d’échange au Vaudreuil (Val de Reuil).
Partager l’article
Romain VEILLON – GSK VACCINES
Références
[1] : UPS<790><1790>, www.usppf.com
[2] : WHO, Visual inspection of particulate matter in injectable preparations http://apps.who.int/phint/en/p/docf/
[3] : Knapp JZ., The scientific basis for visible particle inspection.,PDA J Pharm Sci Technol. 1999 Nov-Dec;53(6):291-302.
[4] : VeillonR., PDA conference Bethesda 4thOct 2011, MVI performance as a baseline for AVI.
[5] : Melchore JA, Sound practices for consistent human visual inspection. AAPSPharmSciTech. 2011 Mar;12(1):215-21.