Sommaire
- Dormons tranquille jusqu’en 2100 ?
- Deviations et CAPA Mindset Driving System
- Capa, Déviations, Évènements Qualité
- CAPA et Déviations
- Nouveau QMS ? Attention à ces points pour réussir !
- Validation of the Imaging Technology for a novel microbiological colony counter
- Technologies Barriere & révision de l’Annexe 1 : exigences & réponses opérationnelles pour les industriels
- BPF Annexe 1 et lyophilisation
CAPA et Déviations
Le traitement des CAPA se situe au cœur du système qualité. Pour autant, sa mise en œuvre est difficile au quotidien, tant pour le Laboratoire fabricant que pour ses sous-traitants et fournisseurs. L’utilisation d’un e-QMS est un avantage indéniable pour prévenir les principales déviations rencontrées. Nous détaillons ici ces déviations, ainsi que les avantages et inconvénients des solutions e-QMS par abonnement ou installées en local.
1. Les déviations rencontrées dans le traitement des CAPA
a. Les déviations qui concernent le laboratoire en interne
Il serait sans doute illusoire de vouloir lister ici toutes les déviations constatées sur la gestion des CAPA Les Warning Letters de la FDA, les injonctions des Autorités Compétentes européennes nous fournissent de nombreux exemples à ce sujet, sans compter les nombreux rapports d’inspection où des points en rapport avec le traitement des CAPA figurent très souvent. Nous ne citerons ici que les principales, à titre d’illustration.
Parmi celles-ci, le délai de traitement des CAPA est sans doute une des déviations les plus fréquentes. Nous avons souvent tendance à surestimer nos capacités à traiter une CAPA dans les délais que nous nous sommes fixés, ce qui revient à sous-estimer le temps de traitement réel, et plus encore à sous-estimer les autres CAPA qui vont inévitablement se greffer le temps que la CAPA en question soit traitée et clôturée. Les e-QMS procurent un accès beaucoup plus facile aux CAPA en cours, aux répartitions des responsabilités, et aux moyens attribués pour leur traitement. Elles permettent d’avoir cette vision d’ensemble sur l’estimation du temps de traitement de la CAPA qui doit être lancée, et le temps qui a déjà été alloué aux autres CAPA en cours.
L’impact vis-à-vis de ces autres CAPA en cours est aussi une déviation fréquente, difficile à appréhender en système papier. Tout dépend bien sûr de leur nombre, mais ce nombre est généralement conséquent, proportionnel à la taille du site concerné. Plus leur nombre est important, plus il est difficile d’identifier celles qui peuvent être potentiellement impactées par la CAPA qui doit être lancée et d’évaluer la nature exacte de l’impact de cette nouvelle CAPA sur les CAPA déjà en cours.
La meilleure solution reste de regrouper toutes les CAPA dans un seul et même système, plutôt que de séparer les CAPA en fonction de leur origine. À titre d’exemple, nous avons rencontré des CAPA issues d’un audit interne, incohérentes avec des CAPA issues de non-conformités en production. L’origine était certes différente, mais la cause racine était bel et bien identique. Le traitement séparé avait conduit à deux CAPA différentes, pas totalement cohérentes, gérées en parallèle par des personnes différentes.
Un e-QMS permet d’avoir une vision d’ensemble des CAPA en cours et de faciliter l’évaluation de l’impact d’une CAPA potentielle sur les CAPA en cours avant de la lancer. L’usage de mots clés bien définis et bien renseignés dans l’e-QMS est une des clés du succès dans ces études d’impact.
Une déviation heureusement moins fréquente, mais plus compliquée à prévenir : la CAPA est-elle cohérente avec le dossier d’AMM ? La question interpelle, car le dossier d’AMM n’est pas facile d’accès sur les sites de production.
Qui a vu (ou plutôt entrevu) tous les dossiers d’AMM des produits fabriqués sur le site ? Personne ou presque ! Il est compliqué de s’assurer que la CAPA, issue ou non d’un change control, n’impacte pas un voire plusieurs dossiers d’AMM. La CAPA ne risque-t-elle pas d’impacter négativement le produit fabriqué, même s’i elle n’impacte pas l’AMM ? Cette autre évaluation nécessite l’activation d’un circuit d’autant plus complexe que le nombre d’intervenants concernés est important. Là encore, l’outil e-QMS apporte un réel avantage en facilitant la communication avec les experts correspondants des affaires réglementaires, souvent localisés sur d’autres sites.
Lorsque la CAPA est longue à mettre en place, une déviation fréquente est l’évolution de l’objectif en cours de mise en place, souvent pour des raisons motivées. La CAPA réalisée ne correspond plus tout à fait, ou plus du tout, à la CAPA lancée au départ, mais les raisons qui ont conduit à ces évolutions ne sont pas toujours totalement documentées au fil de l’eau. Souvent, la vraie raison est la difficulté pour avoir accès au libellé de la CAPA telle que lancée à l’origine. Le traitement électronique permet d’avoir facilement accès au libellé de la CAPA d’origine, et de pouvoir documenter toute évolution nécessaire, ne serait-ce qu’en faisant référence aux documents qui contiennent les justifications de ces évolutions.
Les analyses de tendances sont nécessaires dans le traitement et le suivi des CAPA, mais difficiles à conduire en format papier car elles nécessitent beaucoup de temps pour saisir les données et les exploiter. Sauf à mobiliser souvent plusieurs équivalents temps plein pour remplir manuellement des tableaux Excel, l’outil e-QMS constitue un gain de temps indéniable pour éviter toute déviation car il fournit instantanément ces analyses de tendances, ce qui permet de se concentrer sur leur traitement.
Une fois mise en œuvre, l’efficience de la CAPA doit être vérifiée, et/ou faire l’objet de validations adéquates. Oui, mais Qui vérifie ? Qui valide ? Quand ? Comment ? et Pourquoi ? Il n’est pas rare que les vérifications ou validations soient incomplètement raccordées à la CAPA, faute d’un outil qui permette de lier facilement les documents et conclusions des vérifications ou validations à la CAPA correspondante. Les critères qui permettent de statuer sur la complétude et l’efficience de la CAPA doivent être clairs, et les responsabilités clairement établies. L’e-QMS permet de conditionner la clôture de la CAPA aux vérifications et/ou validations qui ont été définies au départ, et de définir un circuit décisionnel efficace, sans avoir la nécessité de faire circuler des documents papier.
Enfin, aussi simple que cela puisse paraître, une déviation (trop) fréquente, source d’écarts en inspection, est tout bonnement… le défaut de clôture de la CAPA. Sans un système qui permette un suivi de la CAPA, qui avertisse les personnes concernées, qui génère autant de rappels que nécessaire, il est vite fait d’oublier de clôturer une CAPA noyée dans bien d’autres CAPA ou d’autres tâches en cours. L’outil e-QMS donne une vision claire des CAPA qui sont à clôturer et sous quel délai. Il permet d’améliorer la gestion de ces clôtures en temps et en heure.
b. Les déviations qui concernent les sous-traitants et fournisseurs
Gérer des CAPA en interne n’est pas toujours facile, mais il est autrement plus compliqué de gérer des CAPA qui concernent des sous-traitants et fournisseurs. Les déviations sont globalement les mêmes, mais le circuit fonctionnel met en jeu davantage d’intervenants. Le Laboratoire donneur d’ordre a souvent des moyens limités pour suivre le lancement, la réalisation, la vérification et/ou validation, et finalement la clôture de la CAPA. Tout repose sur la communication avec le sous-traitant ou le fournisseur, effectuée généralement à distance. Avoir un interlocuteur unique chez le sous-traitant ou le fournisseur pour la gestion des CAPA est un plus indéniable, mais cela n’est pas toujours le cas.
Compte tenu de ce contexte, des déviations spécifiques apparaissent. Certaines CAPA de fournisseurs et sous-traitants ne sont pas lancées pour des raisons multiples (manque de temps, de moyens, désaccord avec le donneur d’ordre, …), sans que le donneur d’ordre en soit forcément averti. Les CAPA lancées peuvent être sensiblement différentes de celles convenues. Les critères de vérification ou validation de leur mise en place et de leur efficacité peuvent être jugés inappropriés par le donneur d’ordre. Ces déviations peuvent être mises en évidence par le donneur d’ordre lors du traitement des CAPA, au fil de l’eau, mais il est aussi des cas où ces déviations ne sont mises en évidence que lors d’un audit, longtemps après la clôture de la CAPA.
L’étroitesse des relations entre le donneur d’ordre et son sous-traitant ou fournisseur est la clé du succès. L’outil e-QMS apporte là encore un réel avantage, dans la mesure où il facilite une communication efficace entre le donneur d’ordre et le sous-traitant ou le fournisseur. La situation idéale est que le fournisseur ou le sous-traitant ait un e-QMS dont le module CAPA est compatible avec celui du donneur d’ordre, ou accepte de renseigner des informations directement dans l’e-QMS du donneur d’ordre, si ce dernier lui a ouvert des droits. Mais cela n’est pas toujours possible pour de multiples raisons. Le donneur d’ordre doit s’adapter à cette multiplicité de cas de figure.
c. Validation de l’utilisation de l’application
Le procédé qui permet d’enregistrer les évènements, de gérer le suivi des actions et leur clôture, devra être validé en tenant compte de la nature de l’outil qui est utilisé et la manière dont il fonctionne pour gérer, traiter et sécuriser les informations stockées.
Quels que soient la technologie ou le processus utilisé, un document formalisé présentera le fonctionnement, le traitement et la gestion des informations, ainsi que les rôles et responsabilités dans l’utilisation de l’outil et l’exploitation des informations.
d. Intégrité des données
L’intégrité des informations présentes dans le procédé (Quels que soient la méthode ou le système utilisé), devra être garantie par une série de mesures préventives visant à prévenir :
• Toute modification non maîtrisée et non tracée dans le système,
• Tout effacement non maîtrisé et non tracé dans le système, d’information justifiant la validité des actions correctives et préventives pour maîtriser les écarts.
Le procédé CAPA géré au travers d’un formulaire de type tableur ne garantit pas la sécurisation et l’intégrité des informations au travers d’un jeu de mots de passe. L’outil conçu via un tableur permet tout au plus de sécuriser une saisie accidentelle d’informations dans une cellule contenant une formule, mais n’est absolument pas conçu pour protéger l’intégrité d’informations critiques à lui tout seul. Le formulaire devra être archivé dans un environnement informatique qui le protège de tout effacement non contrôlé ou modification non tracée de son contenu. Une analyse de risque permettant d’évaluer les situations ayant un impact sur la perte de l’information ou la perte de son intégrité permettrait d’identifier et mettre en place un certain nombre de mesures techniques et procédurales, en prenant en compte une question essentielle “Jusqu’à quel niveau de verrouillage de l’outil et de son environnement devrons nous aller, sans contraindre son utilisation et à terme l’abandonner”.
Des solutions applicatives sont disponibles dans le marché, mais au prix d’investissements qui peuvent s’avérer coûteux si le besoin n’est pas formalisé et évalué (Spécifications des Besoins Utilisateur = SBU). Cette alternative n’exempte pas le responsable de son utilisation de valider le procédé en ayant une approche par le risque lié à la manière dont il utilisera la solution informatisée.
Une autre alternative reste l’application utilisée via un abonnement (Cloud/SAAS) comme outil de gestion des CAPA, mais limitée en termes de configuration personnalisable. Elle est cependant paramétrable pour un usage restreint aux utilisateurs disposant de licences proportionnées aux profils (Droits et privilèges) souscrits dans le contrat d’abonnement. La particularité c’est que c’est l’éditeur qui gère l’évolution et les mises à jour de l’application. Comme pour les deux alternatives précédentes, elle devra être soumise à un plan de validation et maintien en état validé, selon les référentiels en vigueur.
La base de données reste la propriété du client utilisateur, même en cas d’interruption de l’abonnement. C’est au client utilisateur qu’il revient de bien encadrer par un contrat de support, la migration de ses données pour une utilisation par une autre solution ou la possibilité d’extraire les informations de la base de données pour les rendre exploitables.
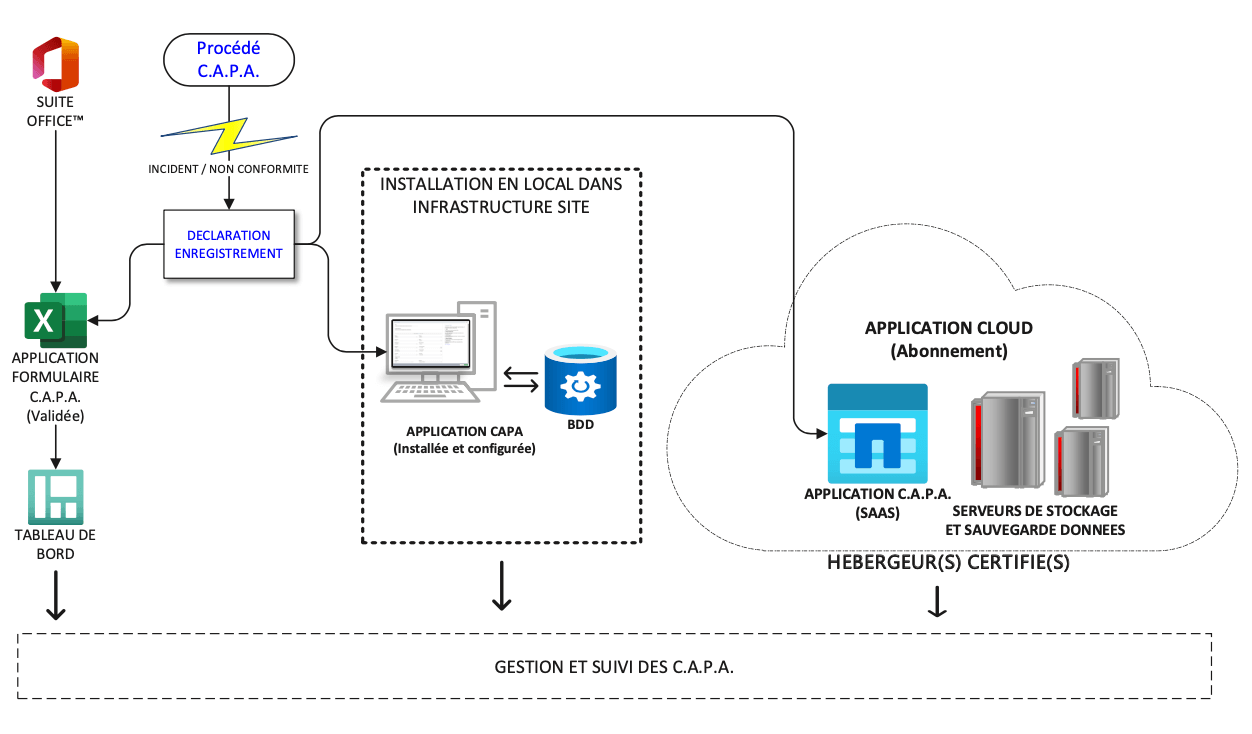
2. Fonctionnement d’une application CAPA par abonnement ou installée informatiquement en local
Lorsque le choix d’une gestion procédurale, via un formulaire développé sur la base d’un tableur n’est pas retenue, les deux alternatives qui présentent le plus d’avantages en termes de protection de l’intégrité des données sont :
• L’application installée et paramétrée à un usage adaptée ou disposant de développement spécifiques qui requiert sa maintenance via un contrat de support,
• L’application paramétrable, fonctionnant par la souscription à un contrat SAAS avec abonnement.
a. Principe de fonctionnement d’un processus CAPA en e-QMS
Solution informatique installée dans l’infrastructure informatique du site utilisateur
L’application informatique paramétrée et installée dans l’infrastructure informatique du client utilisateur est un outil fonctionnant sur la base d’un programme configuré (Sur la base d’une SBU), d’un côté et de l’autre, une base de données contenant tous les enregistrements et informations saisies lors de la déclaration d’un évènement, le suivi et le traitement des actions correctives, jusqu’à leur validation (Clôture). La base de données sera administrée par un référent du département informatique, sous la responsabilité du responsable du procédé (AQ/CQ).
Solution informatique fonctionnant sur le “Cloud” (Mode SAAS)
Cette alternative fonctionne et s’utilise sur le même principe que l’application installée en local sur le site utilisateur. Elle requiert cependant un abonnement proportionné au nombre de licences associées à des droits et autorisations dans le système.
Comme pour l’autre solution installée sur site, c’est une SBU qui fera l’objet d’une revue de conception, pour que le paramétrage personnalisé de son fonctionnement soit adapté à son utilisation encadrée.
Dans cette alternative, la base standard de l’application informatique ne pourra pas être personnalisée spécifiquement aux besoins particuliers puisqu’elle est utilisée, au même moment, par plusieurs sociétés clientes de l’éditeur. À cela s’ajoute le fait que le client utilisateur n’a pas la maîtrise de son évolution ou de sa mise à jour, qui sont gérées par le fournisseur de la solution. Pourtant, comme pour toute autre utilisation d’un système informatisé dans une activité réglementée, c’est l’utilisateur final qui est responsable de la validation du procédé informatisé conformément à la réglementation applicable.
Dans cette alternative il reste le propriétaire de la base de données et de son maintien en état validé. Il devra anticiper, au travers d’un contrat cadre, la méthode dont il peut continuer à exploiter la base de données, en cas de rupture de contrat avec l’éditeur. Pour cela dans la majorité des cas la base de données est soit hébergée dans l’infrastructure informatique interne ou chez un hébergeur avec lequel il devra mettre en place un contrat cadre de sous-traitance (Cf. §2 Annexe 11). Il est indispensable d’anticiper sur la lisibilité des données historiques migrées pour être utilisées par une autre solution informatique.
b. Fourniture de service (Intégration et support)
Le.s prestataire.s externe.s et “interne.s” (DSI), intègre.nt le processus formalisé qui encadre le maintien en état validé de l’habilitation des “utilisateurs clés”, ayant des rôles dans le système qualifié, conformément à la réglementation applicable.
Il est indispensable (voire obligatoire) d’accorder les mêmes contraintes (droits et privilèges), aux prestataires externes qu’aux utilisateurs et détenteurs du procédé de gestion.
c. Validation (cas système acheté ou système en SAAS)
L’utilisation et le fonctionnement de l’application et sa base de données seront intégrées dans un plan de validation basé sur une approche par le risque. Les impacts pris en compte dans l’évaluation de chaque situation de risque liée à son fonctionnement et son utilisation sont essentiellement la perte des informations (dites critiques et décisionnelles) ou la perte de leur intégrité.
L’application informatique et sa base de données constituant l’essentiel du procédé suivent un plan de validation et maintien en état validé adapté à un logiciel de catégorie 4, à minima (Cf. GAMP V). Ce plan de validation initiale, comme le processus de maintien en état validé prennent en compte la documentation de spécification fonctionnelle comme celle qui permet d’utiliser l’application et maintenir sa base de données pendant toute la durée du cycle de vie et au-delà, pendant toute la durée de rétention des données qualité présentes dans la base de données.
Conclusion
Quel que soit la solution informatisée qui est retenue, bien entendu en tenant compte des moyens financiers, centraliser l’e-QMS permettra plus facilement de paramétrer (Pré-sélection) des causes racine types, les activités concernées, les systèmes ou processus sources ou impactés, les procédés, voire le(s) produit(s) de santé impacté(s). Ceci permet facilement au travers d’un paramétrage validé, de pouvoir identifier et classer rapidement et visuellement des causes, des sources, les processus, le(s) fournisseur(s) ou le système, comme leur récurrence et les produits impactés.
Il est plus facile d’identifier et d’analyser les CAPA quand l’outil (e-QMS), peut compiler, filtrer et classer plus rapidement et sans erreur, selon les besoins requis pour mener efficacement, à partir de type d’anomalies, type ou nature des sources racine, fournisseur, activité, système ou produits impactés, des analyses de tendance et mieux cibler le produit, le système ou une source particulière commune. L’application informatique est plus rapide et précise qu’une analyse documentaire qui requiert le “regard affuté” d’une personne expérimentée.
Partager l’article






