Sommaire
- La campagne on y gagne ! Le travail en mode campagne, une avancée sur la productivité des isolateurs.
- Inspection visuelle : principaux constats des inspections de l’ANSM
- Validation des nettoyages des équipements de production : Contrôle visuel, habilitation du personnel au « visuellement propre »
- A Refresher on Disinfectant Wet Contact Time
- RDM et RDIV de l’UE : Les produits combinés désormais soumis au même degré de surveillance que les dispositifs médicaux autonomes
- Fiabilité de la lignée monocytaire Mono-Mac-6 pour la détection des pyrogènes endotoxiniques et non-endotoxiniques
- Indicateurs biologiques, pousses aléatoires - votre cycle de décontamination est-il réellement en cause ?
- Determining a Strategy for Container Closure Integrity Testing of Sterile Injectable Products
- Efficient Control Strategy enabled by structured Knowledge
- Une solution performante pour les dénombrements en temps réel des colonies sur membranes dans l’analyse microbiologique avec ScanStation
Indicateurs biologiques, pousses aléatoires - votre cycle de décontamination est-il réellement en cause ?
Il n’est pas rare, lors des qualifications de performances d’un système de décontamination, d’observer des pousses suite à l’incubation d’indicateurs biologiques. Les investigations menées, suite à ces non-conformités, sont souvent longues, et aboutissent généralement à une remise en cause du cycle développé.
Avez-vous pensé aux ‘Rogues BI’?

1. Qu’est-ce qu’un ‘Rogue BI’?
Un indicateur dit ‘Rogue’, ou ‘coquin’ dans la langue de Molière, est dit d’un indicateur montrant des signes de pousse inexplicables et incohérents après incubation, lors des phases de qualification de performances, ou de développements de cycles. Ces pousses n’ont généralement pas d’explications rationnelles, ne sont pas constantes au fil des cycles réalisés, et surtout vont parfois contre toute logique de résultat attendu. Ces résultats incohérents font perdre du temps lors des investigations menées afin de les expliquer, et retardent les mises en route, ou remise en route, des équipements de production.
Voici quelques pistes à étudier dans les cas ou des résultats d’indicateurs biologiques, paraissent étranges et difficilement explicables.
2. Conséquences des rogues lors d’un développement de cycle.
Elles peuvent être très vastes. Sans cycle de décontamination valide, la production ne peut être lancée ou redémarrée suite à des requalifications, impliquant des coûts importants pour les industriels, sans oublier les problèmes que pourront soulever les autorités règlementaires lors d’audits.
Certains fabricants d’indicateurs, recommandent l’utilisation de triplicats d’indicateurs lors des qualifications (3 indicateurs à la même position), suggérant ainsi que si 1 indicateur pousse sur les 3 à cette position, celle-ci est de fait validée. Bioquell n’est pas tout à fait en accord avec ce procédé. Un témoin positif ne peut être simplement ignoré.La politique de Bioquell à ce sujet est de répéter différents cycles afin de s’assurer que cette pousse est imputable soit au cycle développé, soit à la qualité de l’indicateur biologique utilisé.
3. À quoi les rogues sont-ils dus ?
Bioquell a réalisé une étude impliquant plusieurs industriels commercialisant ces indicateurs, en observant les coupons grâce à un MEB (microscope électronique à balayage). Il est en effet difficile d’étudier les causes amenant à des indicateurs rogues, puisque cela implique de les détruire (mise en incubation). Il faut donc pouvoir les observer avant de les incuber. Les résultats obtenus suggèrent que ces rogues peuvent être induits par quelques problématiques particulières.
3.1 Milieu présent dans l’inoculum(Image 1)
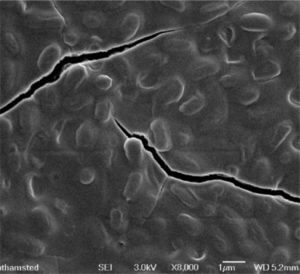
3.2 Disque inox abimé (Image 2)
| Le support est un élément constitutif crucial de l’indicateur, et les dommages sur le disque peuvent aider les spores à survivre. Ces dommages sont souvent des éraflures, ou des enclaves sur la surface du disque, où les spores peuvent trouver refuge, et ainsi être protégés lors du cycle. |
3.3 Agglomération ou multicouche (Image 3)
| La plupart des fabricants d’indicateurs insisteront sur l’importance d’une couche unique et une répartition uniforme de la charge microbienne sur le disque. En effet, l’empilage des couches de spores induit une résistance importante de l’indicateur, puisque le biocide ne pourra passer au travers des multiples couches microbiennes, laissant ainsi non exposées les couches de micro- organismes les plus profondes (~biolfilm). |
4. Quels sont les symptômes typiques des rogues Bi’s ?
4.1 Incohérence des résultats au fil des cycles
L’effet le plus significatif et perturbant dans l’étude des indicateurs rogues, est sans doute l’incohérence des résultats obtenus tout au long des cycles réalisés, notamment lors d’une QP.
Rappel : Nous supposerons ici qu’un seul et unique lot d’indicateurs biologiques est utilisé. Si plusieurs lots d’indicateurs biologiques sont utilisés, notamment lors de qualification de performances, ou toute autre requalification saisonnière, les résultats ne sont pas exploitables.
Cas 1 : Inconstance des résultats sur plusieurs cycles identiques dont les paramètres sont contrôlés et monitorés:
Il peut arriver que sur 3 runs consécutifs, avec le même cycle de référence, et dans des conditions environnementales identiques, les résultats montrent des incohérences notables.
Par exemple : Pousse sur le cycle 2 d’une position qui ne montre pas de signe de pousse aux cycles 1 et 3
- Une autre position montre une pousse seulement au cycle 1
- Une dernière position développe une croissance aux cycles 1 & 3
Après vérification que les cycles réalisés ont bien été identiques en tous points, et que les paramètres environnementaux sont bien respectés, cette variation de résultats peut être expliquée par la présence de rogues Bi’s.
Cas 2 : Indicateurs positifs avec des cycles plus forts, censés être plus efficaces:
Suite à une série infructueuse de tests entrainant des résultats non valides lors de qualifications, le réflexe est bien souvent de renforcer le cycle de décontamination. Quel désastre de s’apercevoir que de nouvelles positions sont positives. Un cycle plus fort, est normalement sensé éliminer les positions non conformes oberservées lors des cycles plus faibles, et non pas apporter de nouvelles incertitudes. Il n’est donc pas logique que de nouvelles positions soient positives alors qu’elles ne l’étaient pas avec les cycles précédents plus faibles.
4.2 Pousses non immédiates
Habituellement, un indicateur positif montre des signes de croissance assez rapidement (j+1 ou j+2) après incubation. Il est plus rare de voir des indicateurs montrer des signes de croissance à j+5 ou j+6. Cela peut être significatif d’indicateurs ‘rogues’. En effet, certaines des causes de rogues observées ci-dessus, montrent qu’ils peuvent parfois être induits par des superpositions de couches de spores, ou par des anfractuosités dans le support, permettant aux spores de se protéger.
Il est donc possible que le phénomène de pousses à j+5 ou j+6, démontre cet effet de protection artificiel des spores non atteintes par la décontamination. L’apparition de positifs en fin de période d’incubation peut s’expliquer par le fait que les couches supérieures de spores détruites mettent du temps à repasser en suspension dans le bouillon, avant de laisser place aux spores non détruites dans les sous-couches protégées. Le milieu de culture met donc plus de temps à atteindre ces spores toujours actives, d’où une latence importante observée lors de l’incubation.
4.3 Comment devrait se présenter un indicateur vu au microscope afin de réduire les risques de rogues ? (Image 4)
Une nouvelle procédure a également été adoptée pour tester les indicateurs Bioquell. Le test KM100, observe la résistance des lots, aidant ainsi à identifier les lots plus résistant que les autres. Le but ici, est d’identifier les lots ayant une résistance de référence (valeur-D) la plus proche possible de celle que bioquell préconise lors de l’utilisation de ses systèmes de décontamination.
Bioquell prend également des clichés MEB d’un échantillon d’indicateurs, sur tous les lots commercialisés, afin de contrôler la répartition et la qualité des indicateurs libérés. Ces images sont disponibles sur demande pour les clients Bioquell, afin de les aider dans leurs démarches qualités. Ce test n’est pas un critère de libération de lots, puisque seule une petite partie de la production est testée, mais contribue aux critères qualités Bioquell.
Néanmoins, et malgré tous les efforts entrepris dans la fabrication des indicateurs, il existera malheureusement toujours des rogues. En effet, les indicateurs sont fabriqués à partir d’un matériel biologique vivant qu’il est difficile de totalement contrôler. Le but de Bioquell est de réduire au maximum la part des rogues au sein des lots commercialisés.
Partager l’article
Jules Boulicot – Bioquell
Jules Boulicot, ingénieur commercial au sein de l’entreprise de Bioquell, est expert en en Désinfection de Surfaces par Voie Aérienne (DSVA). Il occupe un rôle majeur en gestion de projets et en intégration de solutions techniques dans les process critiques clients, pour de multiples acteurs majeurs de la production/R&D pharmaceutique et biotech (équipements et services).
Glossary
References
1978 (US CFR): Section 211.67 added describing equipment cleaning and maintenance
1993 (US FDA guideline): Guide to inspections for cleaning validation2000 (ICH Q7): Guide for active pharmaceutical ingredients
2004 (US FDA guide): Guide to inspections validation of cleaning processes
2010 (PDA): TR 49 – Points to consider for Biotechnology Cleaning Validation
2010 (ISPE): Risk-Based Manufacture of Pharmaceutical Products
2012 (PDA): TR 29 – Points to consider for Cleaning Validation
2015 (EMA): Guideline on setting health based exposure limits for use in risk identification in the manufacture of different medicinal products in shared facilities
2015 (Eudralex Vol. 4 – GMP Guidelines Annex 15): Qualification and Validation