Sommaire
- La campagne on y gagne ! Le travail en mode campagne, une avancée sur la productivité des isolateurs.
- Inspection visuelle : principaux constats des inspections de l’ANSM
- Validation des nettoyages des équipements de production : Contrôle visuel, habilitation du personnel au « visuellement propre »
- A Refresher on Disinfectant Wet Contact Time
- RDM et RDIV de l’UE : Les produits combinés désormais soumis au même degré de surveillance que les dispositifs médicaux autonomes
- Fiabilité de la lignée monocytaire Mono-Mac-6 pour la détection des pyrogènes endotoxiniques et non-endotoxiniques
- Indicateurs biologiques, pousses aléatoires - votre cycle de décontamination est-il réellement en cause ?
- Determining a Strategy for Container Closure Integrity Testing of Sterile Injectable Products
- Efficient Control Strategy enabled by structured Knowledge
- Une solution performante pour les dénombrements en temps réel des colonies sur membranes dans l’analyse microbiologique avec ScanStation
Une solution performante pour les dénombrements en temps réel des colonies sur membranes dans l’analyse microbiologique avec ScanStation.
Le dénombrement des microorganismes viables sur milieux de cultures gélosés reste la méthode de référence recommandée ou imposée par les différentes normes pour les tests microbiologiques en contrôle libératoire. Il s’agit soit d’un ensemencement direct avec un volume de l’échantillon liquide à analyser (étalement en surface du milieu ou inclusion dans un milieu fondu avant sa prise en masse) soit d’une libération de la biomasse de l’échantillon solide dans un volume liquide qui est filtré sur une membrane (diamètre de pores 0,22 à 0,45 µm) qui sera ensuite déposée sur le milieu de culture approprié.
Les milieux sont ensuite incubés à la température permissive pour les microorganismes à isoler et les colonies qui se sont développées (UFC) sont dénombrées en fin d’incubation traditionnellement par comptage manuel par un technicien.
Bien qu’éprouvées, les techniques basées sur la culture peuvent présenter différents biais de la préparation de l’échantillon à la lecture finale des boites (Corry et al., 2007). Si l’on s’intéresse plus particulièrement aux inconvénients liés plus spécifiquement au dénombrement final, les principaux sont :
- Le temps important consacré au dénombrement : le dénombrement est une étape longue où un ou plusieurs techniciens doivent compter chaque UFC développé et ceci pour un nombre de boites de Pétri très importants. Cette activité représente plusieurs heures hebdomadaires dans l’activité d’un laboratoire d’analyses microbiologiques,
- La capacité du technicien à détecter les colonies : et celle-ci peut être impactée par différentes causes uniques ou combinées. Le phénotype des colonies peut rendre compliqué la détection sur un milieu ou une membrane (colonies translucides ou de couleur proche de la membrane ou du milieu). La taille des colonies est également contraignante lorsque celles-ci sont des micro colonies ou au stade précoce de développement. Leur localisation sur les bords des boites de Petri peut également entrainer des omissions de certaines colonies. Enfin, une densité importante des colonies sur le milieu va également compliquer la détection de chaque UCF en tant que telle,
- Le phénomène de confluence pendant l’incubation : La lecture des boites étant réalisée en fin d’incubation (de 24h à plusieurs jours), certaines colonies peuvent être masquées par d’autres ou se chevaucher, rendant leur détection impossible et/ou ne donnant l’impression de la présence d’une seule colonie alors qu’en réalité ce sont plusieurs colonies,
- Le risque d’erreur au comptage : pour partie intrinsèquement lié à deux points cités précédemment, le phénomène d’erreur au comptage notamment lorsque les séries de boites à compter sont importantes est également récurrent et mis en évidence dans de nombreuses études depuis plusieurs décennies (Fowler et al., 1978 ; Peeler et al., 1982).
A ces risques d’erreurs du dénombrement à la paillasse, s’ajoutent ceux liés au traitement du résultat, volontaires ou involontaires: tels que :
- L’erreur de report du résultat,
- L’oubli du report du résultat,
- La falsification de données,
- L’effacement de données,
- La destruction des données.
Depuis quelques années, la réglementation s’est évertuée à imposer la notion d’intégrité des données.
L’intégrité des données fait référence au maintien et à l’assurance de l’exactitude et de la cohérence des données tout au long de leur cycle de vie, de la conception, de la mise en œuvre et de l’utilisation de tout système qui stocke, traite ou récupère des données. L’intégrité des données est une préoccupation réglementaire clé et pour aider les personnes travaillant en production pharmaceutique et les soins de santé, des documents ont été publiés par la Food and Drug Administration (FDA, 2018). Elle est devenue désormais une exigence fondamentale du système qualité pharmaceutique décrit au Chapitre 1 des GMP. Les données se réfèrent au système ALCOA et doivent donc être :
- Attribuables : auteur et source identifiées,
- Lisibles : interprétables et à long terme,
- Contemporaines : enregistrées au moment où elles sont collectées,
- Originales ou de copie certifiée,
- Fiables
Dans ce contexte et pour palier à l’ensemble de ces problématiques, dans une évolution logique des systèmes de détection semi-automatiques ou automatiques qui sont apparus depuis un peu plus de 20 ans, l’émergence de technologies de comptage automatisé avec une gestion informatisée des données à vue le jour. Parmi ces technologies, nous étudierons l’exemple du ScanStation développé par Interscience.
1. Présentation du ScanStation
ScanStation, station d’incubation et de comptage de colonies en temps réel, détecte et compte les colonies dès leur apparition pour 100, 200 ou 300 boîtes de Petri. ScanStation permet la lecture microbienne en temps réel pendant l’incubation. Il fournit des résultats microbiens complets et anticipés pour les laboratoires de contrôle qualité et R&D des industries pharmaceutiques intégrant, une traçabilité complète des données en conformité avec le 21 CFR part 11.
ScanStation a été conçu et développé par Interscience, une société française. L’innovation majeure de ScanStation est de réaliser le comptage automatique des colonies à un stade précoce de leur développement, dès le début du cycle d’incubation. Les boites de Petri sont prises en photo à intervalle régulier, toutes les 30 minutes, (toutes les heures pour le modèle ScanStation 300) délivrant une vidéo de la croissance microbienne. Le résultat final est ainsi connu jusqu’à trois fois plus rapidement par un comptage automatique des colonies, supprimant le travail répétitif, et en dissociant les artéfacts d’origine donc offrant un résultat plus précis et beaucoup plus tôt. La vidéo de croissance accélérée permet de « remonter le temps » et aide à valider les résultats, car l’opérateur peut revoir les premières images afin de déterminer le nombre initial de colonies, identifié par une croix verte.
2. Objectif de l’étude : Vérification de la performance de détection/dénombrement des colonies sur membranes de filtration par ScanStation
Si la validation de la détection des colonies sur des milieux gélosés est validée, la question de la performance de détection sur des membranes de filtration restait à vérifier. De premiers essais avaient été réalisés par Interscience mais uniquement sur des membranes en cellulose. Des travaux préalables dans le cadre de la collaboration Aptar pharma / Interscience, ont permis des améliorations logicielles permettant une détection des colonies sur des membranes en nitrate, acétate et esters de cellulose couramment utilisées en analyses microbiologiques. L’objectif de l’étude suivante est de vérifier les performances de l’appareil pour une détection des UFC sur membranes notamment en définissant :
- Le type de membrane et le programme de l’appareil permettant le meilleur dénombrement,
- Son aptitude à dénombrer des souches bactériennes de phénotypes différents,
- Son seuil de détection maximal et s’assurer que celui-ci est suffisant pour réussir à dénombrer quantitativement un nombre de colonies important proche des 150 UFC (valeur admise comme seuil maximal dénombrable sur membranes).
3. Matériels & Méthodes
3.1 Membranes testées
Quatre références de membranes couramment utilisées dans les contrôles de microbiologiques sont testées :
- Membrane blanche quadrillée en nitrate de cellulose, 0,45µm (Microsart® Sartorius référence : 16D01–25-06–BK)
- Membrane blanche non quadrillée en acétate de cellulose, 0,45µm (Sartorius référence : 11106–47——N)
- Membrane noire quadrillée en nitrate de cellulose, 0,45µm (Sartorius référence : 16D03–25-H6–BK)
- Membrane noire non quadrillée en esters de cellulose, 0,45µm (Millipore référence : HABP04700)
3.2 Souches microbiennes utilisées
Sept souches sont utilisées dont cinq référencées par la Pharmacopée :
- Aspergillus brasiliensis (moisissure) en BioBall 550 (bioMérieux référence : 56011)
- Bacillus subtilis (bactérie) en Bioball 550 (bioMérieux référence : 56012)
- Candida albicans (levure) en BioBall 550 (bioMérieux référence : 56013)
- Pseudomonas aeruginosa (bactérie) en BioBall 550 (bioMérieux référence : 56017)
- Staphylococcus aureus (bactérie) en BioBall 550 (bioMérieux référence : 56019)
Deux souches isolées des environnements de production (zones non stériles) appelées U1 (colonies beiges translucides) et U2 (colonies blanches).
Les différents essais consistent :
- En des inoculums purs pour chaque souche
- En inoculums contenant aureus (33%), B. subtilis (33%) et P. aeruginosa (33%) (Consortium 1)
- En inoculums contenant aureus (25%), B. subtilis (25%) et P. aeruginosa (25%) A. brasiliensis (25%) (Consortium 2)
3.3 Génération des inoculums et ensemencements des membranes
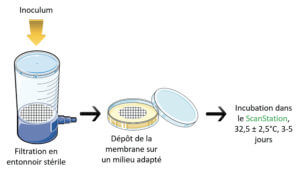
Le protocole d’ensemencement des membranes est résumé dans la Figure 1.
L’inoculum de départ est préparé et amené à la concentration souhaitée. Il est dilué dans un volume de 100 mL de solution saline (0,9%) versé dans l’entonnoir de filtration. Ce volume est filtré au travers de la membrane. La membrane est ensuite prélevée et déposée sur le milieu de culture adapté : TSA-agar pour les bactéries et les consortiums microbiens, et SAB-agar pour les souches de moisissures et levures en cultures pures. Les milieux sont mis en incubation dans ScanStation à 32,5±2,5 °C pendant 3 à 5 jours.
3.4 Détermination des couples « membrane / programme de détection du Scanstation »
ScanStation dispose de différents réglages d’incubation. Ceux-ci font varier l’éclairage des boîtes lors de l’acquisition photographique ainsi que l’algorithme de détection des colonies par le logiciel de traitement d’image. Il existe trois réglages prédéfinis pour les membranes :
- Membrane de filtration blanche papier
- Membrane de filtration blanche polycarbonate
- Membrane de filtration noire
Un premier test réalisé avec S. aureus permet d’affilier le programme du ScanStation qui permet la détection la plus optimale pour chaque type de membrane.
Un inoculum commun est utilisé et des fractions de celui-ci sont dilués dans un volume de solution saline 0,9% stérile (100 mL). Ils sont filtrés sur chaque type de membrane. Celles-ci sont ensuite déposées sur des milieux TSA-agar puis incubées dans ScanStation à 32,5±2,5 °C pendant 3 jours. Chaque essai est composé d’une série de 5 membranes pour chaque référence de membrane.
Un comptage manuel est réalisé en double afin de déterminer le nombre total de colonies développées sur chaque membrane à l’aide des images prises par l’appareil.
3.5 Détermination du meilleur couple « membrane / programme de détection du ScanStation »
Pour chaque couple programme ScanStation / membrane, des essais de détection sont réalisés avec avec S. aureus, B. subtilis et les deux souches usines U1 et U2. Les inoculums et les incubations sont réalisés comme décrits dans le paragraphe précédent. Les séries sont composées également de 5 membranes.
Un comptage manuel est réalisé en double afin de déterminer le nombre total de colonies développées sur chaque membrane à l’aide des images prises par l’appareil.
3.6 Limite de détection maximale
Des séries d’inoculums purs, de S. aureus, B. subtilis ou P. aeruginosa, obtenues par dilution en cascade au 1/10ème, ont servi pour ensemencer des membranes noires quadrillées en nitrate de cellulose. Celles-ci sont déposées sur milieu de culture gélosé type TSA puis mises en incubation dans ScanStation comme décrit précédemment.
4. Résultats et discussions
Les données obtenues sont converties en pourcentages et les résultats présentés correspondent à la moyenne des ces valeurs par série. Idéalement pour considérer une détection efficace, le constructeur se fixe un pourcentage de détection de 95 ± 5%.
4.1 Détermination des couples « membrane / programme de détection du ScanStation »
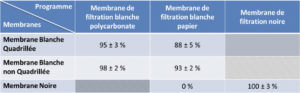
Une première série d’essais a pour but de déterminer quel programme permet une détection en fonction de la membrane utilisée. On note que le programme « membrane de filtration blanche polycarbonate » permet la détection des colonies la plus efficace lorsqu’on utilise des membranes blanches quadrillées ou non (Tableau I) avec des pourcentages de détection respectifs de 95 ± 3 % et 98 ± 2 %. Pour les membranes noires, le programme « membrane de filtration noire » permet une détection totale. A l’inverse le programme « membrane de filtration blanche papier » ne permet pas de détection des colonies malgré le contraste marqué entre la couleur de la membrane (noire) et celle des colonies (jaune) (Figure 2).
Pour les essais suivants le programme « membrane de filtration blanche polycarbonate » est utilisé pour une détection sur les membranes blanches et le programme « membrane de filtration noire » est utilisé pour une détection sur des membranes noires.
4.2 Choix du couple « programme ScanStation/ membrane » le plus optimal pour la détection des colonies
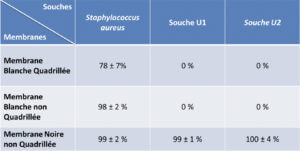
Trois souches bactériennes ont été testées afin de savoir quel couple programme/ membrane était le plus performant pour détecter des colonies de phénotypes très différents (Tableau II). Pour S. aureus, on note des détections de l’ordre de 99 ± 2 % et 98 ± 2 % respectivement pour les membranes noires et les membranes blanches non quadrillées. Pour les membranes blanches quadrillées, le pourcentage de détection est inférieur aux deux autres avec 78± 7 %. Notons que des essais menés avec B. subtilis sur des membranes blanches quadrillées ou non, montraient cette même tendance. En effet le taux de détection passe de 70 ± 2 % sur des membranes non quadrillées à 19 ± 8 % sur membranes quadrillées. L’analyse des images a permis de montrer que les colonies non détectées étaient systématiquement localisées sur les quadrillages. Il y a donc un effet délétère des quadrillages sur les performances de détection dont il convient de tenir compte pour le choix des membranes blanches.
Pour les deux souches isolées des usines (U1 et U2), seules les membranes noires permettent une détection et un dénombrement des colonies de l’ordre de 99 ± 1 % pour la souche U1 et 100 ± 4 % pour la souche U2. Aucune détection de ces souches de couleurs claires, n’est observée sur des membranes blanches.
Considérant ces résultats, le choix des membranes noires couplées au programme du ScanStation « membrane de filtration noire » est la combinaison qui semble être le plus adaptée pour détecter différents phénotypes de façon performante.
Ces résultats ont été confirmés par d’autres séries d’essais sur deux références de membranes de filtration noires (membranes non quadrillées, Millipore et membranes quadrillées, Sartorius) avec des souches pures et des consortiums mimant une population mixte comme on peut en trouver sur les cultures issues des contrôles (Tableau III). Les pourcentages de détection sur les membranes noires Sartorius et Millipore sont comparables et respectivement de :
- 100 ± 2 % et 101 ± 2 % pour aureus
- 100 ± 1 % et 100 % pour subtilis
- 96 ± 4 % et 88 ± 8 % pour aeruginosa
- 100 % pour albicans

Les pourcentages de détection de P. aeruginosa sont plus faibles car les colonies sont parfois translucides. Ce phénotype peut faire qu’il y a peu de contraste avec la membrane ce qui peut limiter le discernement de certaines colonies par le logiciel. De plus, l’analyse des images a montré qu’une partie des colonies non dénombrées étaient proches d’une autre. Cela créé de la confluence et empêche le dénombrement des deux colonies séparément.
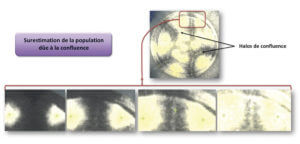
Les pourcentages de détection d’A. brasiliensis montrent une grande variabilité de détection sur les deux types de membranes, égales à 110 ± 17 % (membrane Sartorius) et 161 ± 31 % (membrane millipore). Cette moisissure est blanche et invasive. Sa capacité à se répandre sur la membrane créée une confluence entre les colonies. Cela augmente la densité de mycélium au niveau des zones de confluence et donc une intensification de la couleur blanche. Cette variation de couleur est détectée par le logiciel et une colonie est alors dénombrée par erreur (Figure 3). La première photographie de la Figure 3 montre une membrane noire recouverte par des colonies d’A. brasiliensis. Des halos de confluence y sont visibles.
S’agissant des dénombrements des consortiums 1 et 2, les pourcentages de détection sont de :
- 96 ± 2% sur les membranes Sartorius et de 100 ± 9% sur les membranes Millipore pour le Consortium 1,
- 101 ± 6% sur les membranes Sartorius et 112 ± 21% sur les membranes Millipore pour le Consortium 2.
Les dénombrements des consortiums microbiens présentent des pourcentages de détection proches. L’écart entre le nombre réel de colonies et le nombre de colonies dénombrées est inférieur à 5%. Cependant si l’on analyse les détections par le logiciel sur les images, toutes les colonies ne sont pas dénombrées. Il s’agit d’une compensation numérique. Une erreur de double dénombrement d’une colonie vient compenser une erreur de comptage unique de deux colonies proches. Cette compensation est fréquente notamment lors des dénombrements de B. subtilis dans le consortium. L’erreur est mineure mais répétée au cours des analyses, en revanche ce genre d’erreur est rapidement corrigée par la vérification finale du technicien sur l’écran en fin d’incubation.
De la même façon, le même phénomène est observé pour la détection d’A. brasiliensis. Le nombre de colonies semble plus surestimé sur les membranes Millipore que sur les membranes Sartorius. Il est difficile d’expliquer cette observation. Une hypothèse serait que la membrane peut avoir une incidence sur le phénotype des colonies d’A. brasiliensis. Cette différence d’aspect pourrait influencer la détection des colonies par le logiciel du ScanStation.
4.3 Limite de détection/comptage maximal sur membrane
La limite de détection correspond au nombre de colonies maximal dénombrable sur une membrane de manière quantitative et fiable par le ScanStation.
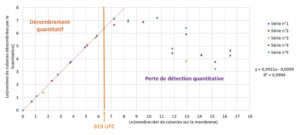
Le dénombrement manuel est effectué en complétant le dénombrement du ScanStation. Les colonies non dénombrées sont additionnées à la valeur obtenue automatiquement et les dénombrements multiples d’une même colonie sont soustraits. La compilation graphique des 5 séries indépendants permet de définir une zone où l’on observe une linéarité entre la détection des colonies par le ScanStation et le nombre réellement présent de colonies sur la membrane (Figure 4). Une extrapolation de la zone de perte de linéarité permet de définir de façon approximative une limite de détection maximale de 619 colonies. Considérant qu’au-delà de 150 colonies sur une membrane, celle-ci est considérée comme non comptable, ce résultat met en évidence une performance importante de l’appareil bien au-delà des valeurs maximales exploitables sur membrane de filtration.
Pour confirmer les performances de dénombrement du ScanStation lorsque le nombre de colonies approche de la valeur seuil de 150 UFC, des essais complémentaires ont été réalisés avec des inoculums de S. aureus, B. subtilis et P. aeruginosa. La concentration de ces inoculums est ajustée à 150 UFC. Les pourcentages moyens de dénombrement obtenus sont les suivants :
- aureus: 100%
- subtilis: 98 ± 1%
- aeruginosa: 99 ± 2%
Cela confirme bien la capacité de l’appareil pour une détection d’un nombre important de colonies de phénotypes différents aux valeurs maximales exploitables.
4.4 Erreurs logiciels observées
Différents types d’erreurs de comptage ont pu être faites au fil de nos essais et ainsi recensées pour aider Interscience à améliorer son interface logicielle. Ces observations sont présentées dans le tableau IV. Le double dénombrement de colonies (161 occurrences) et le comptage unique de deux colonies très proches/confluentes (49 occurrences) sont les plus présentes. Cela représente des survenues d’erreurs sur un total de 3928 colonies dénombrées réparties sur 122 boîtes, soit des pourcentages respectifs de 4% et 1,2%. C’est donc une probabilité d’erreur peu importante et ces occurrences sont finalement corrigeables aisément grâce au double contrôle que le technicien effectue en fin d’incubation sur l’écran de l’appareil pour valider le résultat.

Conclusion
Cette étude permet de confirmer les capacités des incubateurs de la gamme ScanStation pour une détection des colonies microbiennes sur membranes. Il convient de noter qu’en l’état actuel de la solution logicielle embarquée dans l’appareil, la détection n’est efficace que si l’on utilise des membranes de filtration de couleur noire avec le programme de l’appareil « membrane de filtration noire ». Il sera cependant important de tester plusieurs références de membranes noires afin de choisir celle permettant le développement de la plus grande part de la microflore à détecter. Cette étape incontournable reste cependant une validation assez supportable pour un laboratoire puisqu’elle ne demande que de vérifier un élément précis et non l’ensemble d’une technique.
Les performances de détection/ comptage sont d’ailleurs largement suffisantes puisque la détection est quantitative pour des nombres de colonies supérieurs ou égaux à 150, qui reste la valeur maximale que l’on définit sur une membrane en analyse microbiologique.
Au cours de ces essais, différentes erreurs de détection et comptage ont pu être recensées. Elles restent finalement mineures comparées au volume de boites analysées. L’amélioration logicielle continue proposée par le fournisseur pourra probablement permettre d’en résoudre une majeure partie. Ces erreurs sont d’autant plus à relativiser, qu’en plus de leur faible occurrence, en fin d’incubation, une vérification des analyses photographiques et des détections de colonies sont contrôlées par un technicien qui pourra repérer et corriger ces anomalies de comptage au travers d’une interface informatique où la moindre modification d’analyse est tracée et sécurisée.
C’est donc une véritable solution technique en phase avec (1) les exigences de la « data integrity », (2) les exigences de précisions du résultat d’analyse et (3) qui permettra de libérer un temps d’activité technicien considérable qui pourra être dédié à des activités toujours plus grandissantes dans les laboratoires d’analyses microbiologiques.
Partager l’article
Sébastien Bonot – Aptar Pharma
Gautier Varin – Aptar Pharma
Manon Laborie – Interscience
Glossaire
FDA : Food Drug Administration
SAB : sabouraud dextrose
TNCT : Too number to count
TSA : gélose trypticase soja
UCF : Unité formant colonie
Références
Corry J. E. L., Jarvis B., Passmore S., Hedges A., 2007, A critical review of measurement uncertainty in the enumeration of food micro-organisms, Food Microbiology, 24, 230-253.
FDA, 2018, Data Integrity and Compliance With Drug CGMP Questions and Answers Guidance for Industry, https://www.fda.gov/regulatory-information/search-fda-guidance-documents/data-integrity-and-compliance-drug-cgmp-questions-and-answers-guidance-industry
Fowler, J.L., Clark, W.S., Foster, J.F., Hopkins, A., 1978. Analyst variation in doing the standard plate count as described in Standard Methods for the Examination of Dairy Products. J. Food Prot. 41, 4–7.
Peeler, J.T., Leslie, J.E., Danielson, J.W., Messer, J.W., 1982. Replicate counting errors by analysts and bacterial colony counters. J. Food Prot. 45, 238–240.