Sommaire
- La campagne on y gagne ! Le travail en mode campagne, une avancée sur la productivité des isolateurs.
- Inspection visuelle : principaux constats des inspections de l’ANSM
- Validation des nettoyages des équipements de production : Contrôle visuel, habilitation du personnel au « visuellement propre »
- A Refresher on Disinfectant Wet Contact Time
- RDM et RDIV de l’UE : Les produits combinés désormais soumis au même degré de surveillance que les dispositifs médicaux autonomes
- Fiabilité de la lignée monocytaire Mono-Mac-6 pour la détection des pyrogènes endotoxiniques et non-endotoxiniques
- Indicateurs biologiques, pousses aléatoires - votre cycle de décontamination est-il réellement en cause ?
- Determining a Strategy for Container Closure Integrity Testing of Sterile Injectable Products
- Efficient Control Strategy enabled by structured Knowledge
- Une solution performante pour les dénombrements en temps réel des colonies sur membranes dans l’analyse microbiologique avec ScanStation
Validation des nettoyages des équipements de production : Contrôle visuel, habilitation du personnel au « visuellement propre »
Le nettoyage des équipements de fabrication est un aspect fondamental des GMPs afin d’éviter toute contamination croisée des produits pharmaceutiques au cours de leur fabrication. La validation des processus de nettoyage est requise depuis longtemps dans les industries cGMP et est reconnue comme une activité importante pour maitriser le risque de contamination des produits et ainsi assurer leur qualité mais surtout assurer la sécurité des patients.

Les validations de nettoyage tendent à prouver que les méthodes de nettoyage sont efficaces, fiables, robustes et capables d’éliminer des contaminations jusqu’à un niveau fixé.
Une inspection visuelle des équipements est requise par la réglementation après les étapes de nettoyage mais aussi avant le début de la production.
L’inspection visuelle fait partie du nettoyage de routine et constitue le premier critère de validation du nettoyage. Les résultats de cette inspection doivent être jugés acceptables avant de pouvoir prélever des échantillons par écouvillonnage ou par d’autres méthodes sur l’équipement nettoyé en vue d’une confirmation analytique.
Depuis les années 90, plusieurs publications (1), (2), (3), (4), (5), (6) ont abordé le thème de l’étude de l’inspection visuelle annonçant que la limite de détection se situerait dans un range de concentration allant d’environ 1 µg/cm2 à plus de 10 µg/cm2 selon les produits étudiés et les conditions de contrôles. La réglementation US (7) requiert « une inspection des équipements de fabrication immédiatement avant utilisation ». Le PIC/S (8) conseille de réaliser « une étude de contamination sur surface afin de déterminer la concentration à laquelle la plupart des ingrédients sont visibles ».
Le dernier texte de l’EMA Q&A 8 (9) précise que dans le cadre du contrôle des nettoyages après validation et dans certains cas précis « le personnel réalisant les inspections visuelles doit recevoir une formation spécifique et un contrôle régulier de l’acuité visuelle. Et que l’habilitation doit être prouvée par des essais pratiques ».
Cette technique est donc importante à prendre en considération et il est primordial de pouvoir justifier que ces contrôles sont réalisés dans de bonnes conditions. Elle doit être encadrée par un système qualité adéquat.
L’inspection visuelle doit être réalisée sur les surfaces des équipements en contact direct et indirect avec le produit et requiert que ces surfaces soient visiblement accessibles. Dans le cas où les surfaces ne sont pas visuellement accessibles, il est recommandé de pouvoir démonter l’équipement pour y accéder ou d’utiliser des sources lumineuses, miroirs ou endoscopes.
Les résidus ou défauts recherchés peuvent être de différentes sources : produits précédents, agents de nettoyage, contamination microbienne, usure de l’équipement (ex : rayure, rouging, etc.), matières étrangères, liquides techniques (types huiles ou graisses), résidus de solvant de rinçage (ex : eau résiduelle), etc.
En routine, cette inspection visuelle est réalisée sur les équipements par une multitude de personnes en cours ou en fin d’utilisation, après un nettoyage automatique (nettoyage en place), semi-automatique ou manuel, sur des grandes surfaces ou sur des petites pièces nettoyées en laveur. Ces contrôles sont tracés le plus souvent dans des checklists laissées sur l’équipement jusqu’à utilisation, puis jointes au dossier de lot et dans des documents qualité internes au site afin de justifier que les équipements sont propres et utilisables pour une prochaine production.
En début de production, les équipes réalisent aussi un contrôle visuel des équipements. Ces informations sont aussi tracées dans les dossiers de lot et dans des carnets de bord d’équipements ou de zones de production.
La plupart du temps, un premier contrôle est réalisé en fin de nettoyage par une personne et juste avant la réutilisation de l’équipement par une seconde personne différente de la première.
Les équipes qualité et qualification/validation inspectent aussi régulièrement les équipements dans le cadre de leurs activités.
Très souvent, la formation et l’habilitation au contrôle visuel de ces personnes ne sont pas tracées de façon convenable et considérées comme une activité critique lors des habilitations et fait souvent partie de la formation et l’habilitation globale au poste de travail.
De même, dans le cadre de la mise en place des validations de nettoyage, les préleveurs qui réalisent les écouvillonnages, les prélèvements des eaux de rinçage ou les prélèvements microbiologiques sont spécifiquement formés et habilités de façon officielle (ex : essais de recouvrement en laboratoire).
L’habilitation au contrôle visuel devrait alors être référencée et réalisée au même titre que les autres habilitations effectuées sur le site et considérées comme aussi importantes.
Cet article détaille une des approches possibles de la mise en œuvre, la gestion et le suivi de l’habilitation des équipes aux inspections visuelles dans le cadre des validations de nettoyage et contrôle de routine des équipements.
Il décrit les grandes lignes d’une approche qui peut être adaptée, optimisée et modifiée de façon à pouvoir s’appliquer aux procédés internes de chaque site.
Cette habilitation ne peut pas justifier le fait que seule l’inspection visuelle est prise en compte pour statuer sur la conformité des nettoyages.
Cette habilitation permet de justifier que le personnel formé sera capable de détecter visuellement une contamination de surface inférieure à la limite de contamination acceptable, définir le statut propre des équipements et dans ce sens, confirmer que le risque de contamination croisée des équipements est maîtrisé.
Il faut différencier la qualification des principes d’inspection visuelle de l’habilitation du personnel. L’habilitation des équipes est l’étape finale de la mise en place de la stratégie globale d’inspection visuelle. Il va falloir au préalable déterminer les limites d’acceptation des résidus sur les surfaces des équipements, puis déterminer la limite de détection visuelle avant de pouvoir mettre en place le processus d’habilitation des équipes.
La qualification des principes d’inspection visuelle devrait être validée avant la réalisation des essais d’habilitation des équipes (10).
L’implémentation de l’habilitation à l’inspection visuelle nécessite une organisation transverse. Elle est réalisée sur de petits groupes de personnes (opérateurs de production, préleveurs, etc.) et sous la responsabilité du service Assurance Qualité. Le test est développé la plupart du temps par le laboratoire qui possède les moyens de mener à bien la mise en place de ces tests (produits, solvant, coupons des différents matériaux, etc.).
En routine, l’inspection visuelle est différente quand le contrôle est effectué sur de petites pièces qui peuvent être placées dans des conditions idéales de test (angle, luminosité, distance) contrairement au contrôle réalisé sur des équipements volumineux et fixes dont les paramètres de contrôle seront plus restrictifs (angle fixe et non optimal par rapport à la lumière, luminosité faible à l’intérieur de tubes ou grands contenants et distance éloignée des surfaces).
Afin d’homogénéiser l’approche de qualification et d’habilitation, les tests sont réalisés sur des coupons de taille définie (ex : coupon de 100 cm2), de matière et de qualité de surface le plus proche possible des matériaux rencontrés en production. Les tests sont classiquement réalisés avec des coupons en inox, verre et téflon.
Les critères d’acceptation de l’inspection visuelle doivent être définis pour tout contaminant potentiellement présent sur les équipements : résidus de substances actives, de produits finis ou agents de nettoyage. Il n’est pas nécessaire de réaliser les tests de « visuellement propre » pour la contamination microbienne car cette dernière est étroitement liée aux résidus d’autres produits qui resteraient sur les surfaces.
1. Détermination de la limite résiduelle détectable (VRL)
La première étape de la stratégie d’inspection visuelle est la définition de la limite résiduelle détectable, c’est-à-dire la plus petite concentration de produit qui peut être repérable par l’œil humain à la surface d’un matériau.
Le marqueur à utiliser en priorité pour ces tests est le produit issu de l’analyse de risque « Worst case » détaillé dans la stratégie des validations de nettoyage (ex : plan maître de validation de nettoyage), c’est-à-dire la matière première, substance active, produit fini ou résidu le plus dur à nettoyer de chaque famille de produit définie. Si la mise en œuvre du produit fini contenant la substance active la plus difficile à nettoyer est plus facile à mettre en œuvre, alors ce produit fini peut être utilisé pour les tests et inversement. Le choix du contaminant pour réaliser l’étude doit être justifié.
Plusieurs concentrations doivent être étudiées. Il est nécessaire de déterminer dans un premier temps la limite d’acceptation de surface (Limit acceptance surface : LAS qui est évaluée en µg/cm2) selon les approches toxicologiques et thérapeutiques des produits fabriqués. Ces critères d’acceptation sont normalement définis lors de la mise en place des validations de nettoyage et dont la valeur est calculée selon les préconisations du plan maitre de validation de nettoyage.
Dans un second temps, la limite de détection visuelle VRL (visual residual limit en µg/cm2) doit être définie.
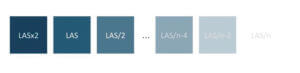
Il est préconisé de déposer, sur coupon des différents matériaux, des concentrations plus ou moins diluées de la concentration LAS et jusqu’à une concentration très faible (ex : plusieurs dilutions successives au 1/10e ou au 1/2e). Ces concentrations sont à définir et à ajuster par l’équipe mettant en œuvre le test sur site.
Un nombre de coupons suffisant doit être mis en œuvre afin d’avoir une représentativité de la gamme de concentration étudiée : une dizaine de plaques au minimum est convenable.
Le dépôt est réalisé préférablement à l’aide d’un spray pour qu’il soit homogène sur la surface du coupon et entre les coupons. Le dépôt à l’aide d’une pipette peut provoquer des amas de produit qui sont difficilement répétables d’un dépôt à l’autre. Les dépôts doivent être secs et réalisés le plus proche possible des tests de visualisation. Il est possible de réaliser au préalable une étude de stabilité de l’aspect visuel des résidus sur les surfaces afin de pouvoir garder les coupons surchargés un temps défini après dépôt.
Il est conseillé de réaliser le test dans des conditions de luminosité proches de celles rencontrées en zone de production. La luminosité peut être relevée dans les différentes zones de production et un range de luminosité peut être pris en considération pour réaliser les tests de qualification et d’habilitation.
Les coupons peuvent être disposés par ordre décroissant de concentration sur une surface plane, avec une luminosité proche de celle des zones de production. Relever et reporter la luminosité au niveau de chaque coupon sur les fiches de résultats avant le test.
Un nombre suffisant (le plus grand possible) de personnes doit effectuer le contrôle de ces coupons afin d’avoir une représentativité des résultats. Il est possible de faire intervenir des personnes de différents services, différents âges, de différentes anciennetés au sein de l’entreprise et portant ou non une correction ophtalmique afin d’avoir le plus grand éventail possible de personnes. Le personnel ne doit pas être spécialement formé à l’inspection visuelle pour réaliser ce test.
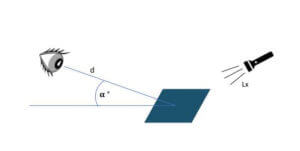
La visualisation doit être réalisée dans des conditions proches de celles des zones de production. Les paramètres importants à considérer sont :
- La distance de vue (d)
- L’angle de vue ()
- La luminosité (Lx)
Ces paramètres de visualisation doivent être au maximum maintenus identiques pour toutes les personnes réalisant le test.
Il est conseillé de réaliser les tests de détermination de la VRL plusieurs fois (par exemple 3 fois) et si possible sur des jours différents afin d’avoir une représentation plus robuste des résultats.
La concentration limite de détection visuelle (VRL) est établie comme étant la concentration la plus faible détectée par 100 % des opérateurs.
La comparaison de la concentration VRL à la concentration LAS permet de déterminer si la limite d’acceptation des résidus sera détectable sur les surfaces des équipements par le personnel réalisant les contrôles.
• Dans le cas où la concentration VRL > LAS, il sera difficile au personnel réalisant les inspections visuelles de détecter la limite de contamination acceptable sur les surfaces en production. Dans ce cas, il est absolument nécessaire de compléter le contrôle visuel par des méthodes analytiques ayant une détectabilité convenable par rapport à la limite LAS.
• Dans le cas où la concentration VRL est proche de la concentration LAS, il est tout de même recommandé de compléter le contrôle visuel par un contrôle analytique ayant une détectabilité convenable.
• Dans le cas où la concentration VRL ≤ LAS (idéalement au-delà d’un facteur 100) (11), le contrôle visuel du personnel sera assez sensible pour détecter la limite de contamination acceptable sur les surfaces. L’habilitation des équipes est alors réalisable par rapport à ces paramètres.
2. Habilitation du personnel
Le but de cette habilitation n’est pas de disqualifier le personnel qui ne réussit pas le test (telle une discrimination opérationnelle) mais d’apporter une formation adéquate pour que tout le monde soit capable de contrôler des surfaces après nettoyage et avoir un contrôle efficace sur l’état de propreté des surfaces.
Avant la réalisation des tests d’habilitation, le personnel doit suivre une formation adéquate sur l’inspection visuelle. Elle peut se dérouler de la façon suivante :
- Lecture des procédures détaillant la réalisation des inspections visuelles,
- Sensibilisation aux types de résidus potentiellement présents après nettoyage sur les surfaces et qui devront être recherchés lors des contrôles,
- Sensibilisation aux équipements. C’est-à-dire connaitre les surfaces des équipements qui seront contrôlées, et connaitre les surfaces difficilement accessibles ou les surfaces nécessitant l’utilisation d’appareil d’aide à l’inspection (endoscope, miroir, etc.),
- Prendre connaissance des tests qui vont être réalisés lors de l’habilitation et les différentes concentration recherchées (VRL, LAS),
- Visualiser des coupons pollués témoins afin d’avoir un recul sur les tests d’habilitation.
Les procédures décrivant l’inspection visuelle doivent être les plus détaillées possible, pouvant inclure des photos, schémas, accessoires et position de contrôle et être compréhensibles afin d’assurer la reproductibilité des contrôles.
De la même façon que la définition de la concentration VRL, des coupons doivent être souillés à l’aide du même produit. Les dépôts doivent être homogènes et secs pour la réalisation des tests.
Les concentrations doivent être adaptées dans l’optique de la réalisation d’un test d’habilitation par rapport à la limite d’acceptation LAS.
Il est conseillé de réaliser les tests avec des coupons souillés à la concentration limite (LAS) et d’autres coupons souillés à une autre concentration qui sera entre la LAS et la concentration limite de détectabilité (VRL). Exemple : 50 % de la LAS ou (VRL+LAS)/2.
Un nombre suffisant de coupons doit être utilisé afin d’avoir une représentativité des résultats (au minimum 10 coupons de chaque concentration).
Des coupons blancs sont préparés par dépôt d’une quantité de solvant pur (correspondant à la quantité de solvant contenu dans la solution de concentration LAS (exemple : eau purifiée ou eau PPI).
Les coupons doivent être identifiés de façon à ce que la personne réalisant le test ne puisse pas détecter le statut du coupon (Propre/sale) et déposés sur une surface plane. Dans le cadre de l’habilitation, les coupons doivent être déposés sur la surface de manière randomisée. La luminosité doit être relevée au niveau de chaque coupon à l’aide d’un luxmètre.
Chaque personne participant à l’habilitation doit vérifier chaque coupon l’un après l’autre dans des conditions de contrôle définies dans la procédures associée (angle, luminosité, distance) et reporter sur une fiche de test le statut de chaque coupon contrôlé : « sale » ou « propre ». Seulement 2 entrées (sale/propre) sont acceptées. Il n’est pas nécessaire de déterminer si certains coupons sont moins ou plus sales que d’autres.
Les coupons souillés à la concentration LAS doivent normalement être identifiés comme sales.
Les coupons souillés à la concentration LAS/2 doivent aussi être identifiés comme sales si cette concentration est supérieure à la VRL.
Les coupons blancs doivent être identifiés comme propres.
Chaque fiche de test est ensuite étudiée et les résultats sont résumés en reportant :
- le pourcentage de détection de coupons sales par rapport aux nombre de coupons réellement sales,
- un pourcentage de détection de coupons propres par rapport aux nombre de coupons réellement propres.
3. Critères d’acceptation
Les résultats attendus suite aux tests d’habilitation du personnel :
Tous les coupons surchargés soient détectés comme « sales » : 100 % des coupons considérés sales
Tous les coupons blancs soient détectés comme « propres » : 100 % des coupons considérés propres
Le terme « propre » est défini comme une absence de résidu visuellement détectable.
Si un coupon « propre » est identifié comme « sale », cela ne doit pas être considéré comme un échec à l’habilitation. Cela peut être dû à une erreur de prudence ou à un léger défaut de surface du coupon en question et ces erreurs peuvent être acceptées. Si plusieurs erreurs (nombre à définir sur chaque site) de ce type sont commises par la personne habilitée, il est alors tout de même important de réaliser une sensibilisation avant de confirmer l’habilitation.
Si un coupon « sale » est identifié comme « propre », alors l’habilitation peut être considérée comme un échec car un équipement visuellement sale pourrait être considéré comme propre et libéré pour une fabrication ultérieure. L’équipement pourrait être utilisé pour fabriquer un produit différent et pourrait être à l’origine d’une contamination croisée entre les fabrications. Dans ce cas précis, la personne devra faire l’objet d’une sensibilisation au contrôle visuel, qui peut être réalisée par le contrôle des coupons utilisés pour l’habilitation à une distance plus proche que celle du test. Cette sensibilisation peut être aussi réalisée par une relecture et/ou une formation individuelle sur la procédure de contrôle. Le test pourra être réitéré afin de confirmer l’habilitation de la personne. Chaque site doit évaluer si la personne est capable de réaliser un contrôle visuel et gérer cette habilitation de la façon la plus déontologique possible.
4. Suivi de l’habilitation
Suite à l’habilitation des équipes, il est nécessaire de contrôler régulièrement si des dérives sont présentes lors des contrôles visuels.
Pour cela, il est recommandé d’auditer régulièrement les équipes lors de la réalisation des contrôles et de participer à des tests de contrôle visuel sur coupon comme détaillé dans le paragraphe précédent. La fréquence de contrôle dépend des pratiques de chaque site.
Si seule l’inspection visuelle est utilisée dans le cadre de contrôle de nettoyage après la validation des procédés de nettoyage, alors le personnel devra subir un contrôle de son acuité visuelle de manière régulière (EMA Q&A8) (9).
Conclusion
La stratégie d’habilitation à l’inspection visuelle dans le cadre des validations de nettoyage ou contrôle de routine des nettoyages est un point très important à considérer et très souvent oubliée ou réalisée de manière très succincte, voire approximative.
Plusieurs groupes scientifiques travaillent actuellement à l’élaboration d’un procédé d’habilitation complet prenant en compte des études statistiques et des tests élargis pour définir les techniques d’habilitation.
Cet article a présenté une des possibilités pour la mise en œuvre, la justification et l’encadrement de l’inspection visuelle et ce d’une façon simple et rapide.
Selon le dernier texte de l’EMA Q&A8 (9), dans certains cas précis, le contrôle visuel pourrait être utilisé seul pour statuer de la propreté de l’équipement en routine après validation de nettoyage (EMA Q&A7) (9). Dans ce cas, la mise en place d’une stratégie d’habilitation visuelle robuste et efficace devra être mise en œuvre et sera attendue par les autorités de santé.
Partager l’article

Christophe Gamblin – Theraxel
Titulaire d’un master scientifique et après plus de 15 ans d’expérience dans l’industrie pharmaceutique en tant que responsable contrôle qualité analytique avec une spécialisation dans la validation des nettoyages, Christophe est maintenant un expert qui accompagne les industriels dans la maitrise de la contamination croisée. Membre de l’organisation ASTM, il participe à l’élaboration de nouvelles normes scientifiques sur le risque chimique dans l’industrie pharmaceutique et biotechnologie.
christophe.gamblin@theraxel.fr
Glossaire
GMP: Good Manufacturing Practices
cGMP: Current Good Manufacturing Practices
LAS : Limit Acceptance Surface (µg/cm2)
VRL : Visual Residual Limit (µg/cm2)
Références
1. Determining Cleaning Validation Acceptance Limits for Pharmaceutical Manufacturing Operations. Fourman, G. L. and Mullen, M. V. 4, 1993, Pharmaceutical Technology, Vol. 17, pp. 54-60.
2. Bestimmung der Sichtbarkeitsgrenzen von pharmazeutischen Feststoffen auf Edelstahloberflächen. Buscalferri, Frank, Lorenzen, Sabine, Schmidt, Michael, Schwarm, Hans-Martin, Anhalt, Ehrhard, et al. 6, 2000, Pharm. Ind., Vol. 62.
3. Cleaning Validation: An Overall Perspective. Jenkins, K. M. and Vander Weilen, A. J. 4, 1994, Pharmaceutical Technology, Vol. 18, pp. 60-73.
4. Visible-Residue Limit for Cleaning Validation and its Potential Application in Pharmaceutical Research Facility. Forsyth, Richard J., Van Nostrand, Vincent, and Martin, Gregory P. 10, 2004, Pharmaceutical Technology, Vol. 28.
5. Using Visible Residue Limits for Introducing New Compounds into a Pharmaceutical Research Facility. Forsyth, Richard J. and Van Nostrand, Vincent. 10, 2005, Pharmaceutical Technology, Vol. 29.
6. Validation of Visual Inspection as an Analytical Method for Cleaning Validation. Desai, Parth and Walsh, Andrew. 2017, Pharmaceutical Online.
7. U.S. Food and Drug Administration. 21 CFR 211.67 (b).
8. Pharmaceutical Inspection Co-operation Scheme (PIC/S).
9. European Medecines Agency (EMA). Questions and answers on implementation of risk-based prevention of cross-contamination in production and ‘Guideline on setting health-based exposure limits for use in risk identification in the manufacture of different medicinal products in shared facili. 2018. EMA/CHMP/CVMP/SWP/246844/2018.
10. Justification and Qualification of Visual Inspection for use in Cleaning Validation for a Low Risk, Multi-Product Facility. Walsh, Andrew, Liu, Dongni (Nina), and Ovais, Mohammad. August 2018, Pharmaceutical Online.
11. Walsh, Andrew, et al. An MSSR-Derived Scale For Assessing Detectability Of Visual Inspection.
12. ASTM International. Standard Guide for Science-Based and Risk-Based Cleaning Process Development and Validation. [Online] 2018. doi: https://doi.org/10.1520/E3106-18E01. doi: https://doi.org/10.1520/E3106-18E01.
13. Agency, European Medicines. Questions and answers on implementation of risk-based prevention of cross-contamination in production and ‘Guideline on setting HBEL for use in risk identification in the manufacture of different medicinal products in shared facilities. 2018.